تعد تقنية التفاعل التحفيزي الكهربائي إحدى الطرق الرئيسية التي تقود مسارات تحويل الطاقة وتنقية البيئة.
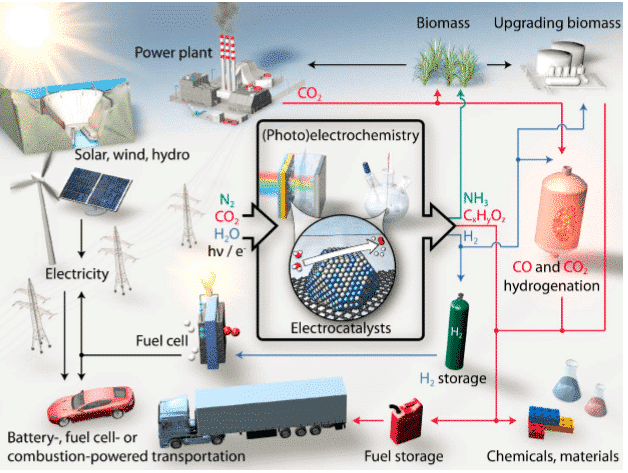
في السنوات الأخيرة ، مع تطور المجتمع وتقدم البشرية ، أصبحت مشاكل الطاقة والبيئة المتزايدة الخطورة مشكلة عالمية تحتاج إلى حل عاجل. يلتزم الناس بالاستخدام الفعال لمصادر الطاقة الجديدة وطرق تنقية البيئة على المدى الطويل. تتضمن طرق البحث الفعالة الحالية لتعزيز تحويل الطاقة وتنقية البيئة العديد من الاتجاهات ، مثل تطوير خلايا الوقود ، وإنتاج الهيدروجين ، ومورد ثاني أكسيد الكربون ، والتحويل الحفاز العضوي لغاز العادم. توفر طرق الاختبار الكهروكيميائية كدليل نظري وسيلة منطقية للتفسير لتطوير أداء الحفاز الكهربائي. يلخص هذا البحث طرق الاختبار الكهروكيميائية المستخدمة بشكل شائع في العديد من التفاعلات الكهروكيميائية.
الشكل 1 عملية التحفيز الكهربائي لتحويل الطاقة المستدامة
1. قياس الفولتميتر الدوري
قياس الفولتميتر الدوري (CV) هو أكثر طرق البحث شيوعًا لتقييم الأنظمة الكهروكيميائية غير المعروفة. يتم الحصول عليها بشكل أساسي من خلال التحكم في إمكانات القطب بمعدلات مختلفة والمسح مرة واحدة أو أكثر باستخدام شكل موجة مثلثة بمرور الوقت. منحنى الجهد الحالي (iE). يمكن أن تحدث تفاعلات اختزال وأكسدة مختلفة بالتناوب على الأقطاب الكهربائية في نطاقات جهد مختلفة. يمكن الحكم على انعكاسية تفاعل القطب الكهربائي وفقًا لشكل المنحنى ؛ يمكن استخدام قمم الامتزاز والامتصاص للمواد المتفاعلة لتقييم المحفز الكهربائي وفقًا لمدى الجهد المحدد. يمكن أيضًا استخدام المنطقة النشطة تحفيزيًا للحصول على معلومات مفيدة حول تفاعلات الأقطاب الكهربائية المعقدة.
الشكل 1.1 مسح منحنى الاستجابة الحالية المحتملة
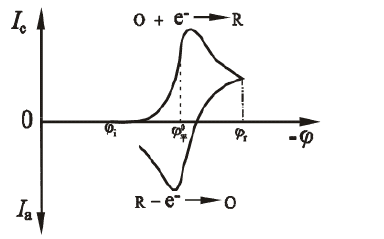
كما هو مبين في الشكل 1.1 ، يتم مسح إمكانات النصف الأول باتجاه القطب السالب ، ويتم تقليل المادة الفعالة كهربيًا على القطب لتوليد موجة اختزال. عندما يتم مسح إمكانات النصف الأخير باتجاه الأنود ، يتأكسد منتج الاختزال مرة أخرى على القطب لتوليد موجة أكسدة. معلمتان مفيدتان لمنحنى الفولتميتر الدوري IE هما نسبة الذروة الحالية ipa / ipc وفرق ذروة الجهد Epa-Epc. بالنسبة لموجة Nernst للمنتج المستقر ، فإن نسبة الذروة الحالية ipa / ipc = 1 ، بغض النظر عن سرعة المسح ومعامل الانتشار وإمكانية التبديل. عندما يتم إيقاف مسح الكاثود ، ينخفض التيار إلى 0 ثم عكس المسح. منحنى iE الذي تم الحصول عليه هو بالضبط نفس منحنى الكاثود ، ولكن يتم رسمه في الاتجاه المعاكس للإحداثيات I و E. تنحرف نسبة ipa / ipc عن 1 ، مما يشير إلى أن عملية القطب الكهربي ليست عملية تفاعل قابلة للعكس تمامًا تتضمن حركيات متجانسة أو مضاعفات أخرى. يمكن استخدام ارتفاع ذروة التفاعل ومنطقة الذروة لتقدير معلمات النظام مثل تركيز الأنواع النشطة كهربيًا أو ثابت السرعة للتفاعل المتجانس المقترن. ومع ذلك ، فإن منحنى السيرة الذاتية ليس طريقة كمية مثالية ، واستخدامه القوي أكثر في قدرته على التحكيم النوعي شبه الكمي.
2-قياس الجهد النبضي
قياس الجهد النبضي هو طريقة قياس كهروكيميائية تعتمد على سلوك الأقطاب الكهربائية. يتم استخدامه لدراسة عملية الأكسدة والاختزال في مختلف الوسائط ، وامتصاص المواد السطحية على المواد المحفزة وآلية نقل الإلكترون على سطح الأقطاب الكهربائية المعدلة كيميائيًا. الاكتشاف فعال بشكل خاص. يشمل قياس الجهد النبضي الخطوة الفولتميترية ، قياس الجهد النبضي التقليدي ، قياس الفولتميتر التفاضلي للنبض ، وقياس الجهد بالموجة المربعة اعتمادًا على الطريقة التي يتم بها مسح الجهد. من بينها ، يشبه قياس الجهد الخطوة طريقة المسح المحتملة ، واستجابة معظم الأنظمة للدقة الأعلى (ΔE <5 مللي فولت) خطوة فولت أمبير تشبه إلى حد بعيد نتائج تجربة المسح الخطي بنفس سرعة المسح.
3. مطيافية المعاوقة الكهروكيميائية
التحليل الطيفي للمقاومة الكهروكيميائية هو تطبيق إشارة كهربائية مضطربة على النظام الكهروكيميائي. على عكس طريقة المسح الخطي ، يكون النظام الكهروكيميائي بعيدًا عن حالة التوازن ، ومن ثم يتم ملاحظة استجابة النظام ، ويتم تحليل الخصائص الكهروكيميائية للنظام بواسطة إشارة الاستجابة الكهربائية. غالبًا ما يستخدم التحليل الطيفي للمقاومة الكهروكيميائية لتحليل وتقييم تفاعل ORR في خلايا وقود PEM ، وتوصيف فقدان الانتشار على سطح مادة المحفز ، وتقدير المقاومة الأومية ، وخصائص مقاومة نقل الشحنة وسعة الطبقة المزدوجة لتقييم وتحسين تجميع القطب الغشاء.
عادة ما يتم رسم طيف المعاوقة في شكل مخطط Bode ومخطط Nyquist. في مخطط Bode ، يتم رسم حجم وطور المعاوقة كدالة للتردد ؛ في مخطط نيكويست ، يتم رسم الجزء التخيلي للمقاومة عند كل نقطة تردد بالنسبة للجزء الحقيقي. يعكس القوس عالي التردد مزيج سعة الطبقة المزدوجة لطبقة المحفز ، ومقاومة نقل الشحنة الفعالة ، والمقاومة الأومية ، والتي تعكس الممانعة الناتجة عن نقل الكتلة. بالنسبة لنظام معين ، لا يتم تعريف المنطقتين بشكل جيد في بعض الأحيان.
الشكل 3.1 طيف الممانعة للنظام الكهروكيميائي
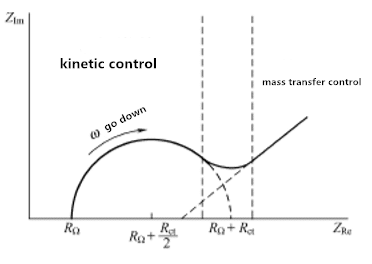
يوضح الشكل 3.1 الخصائص القصوى للتحكم الحركي والتحكم في نقل الكتلة. ومع ذلك ، بالنسبة لأي نظام معين ، ربما لم يتم تحديد المنطقتين بشكل جيد. العامل المحدد هو العلاقة بين مقاومة نقل الشحنة ومقاومة الإرسال. إذا كان النظام الكيميائي بطيئًا في الحركة ، فسيظهر Rct كبير ، والذي يبدو أن منطقة التردد محدودة للغاية. عندما يكون النظام ديناميكيًا ، يلعب نقل المواد دائمًا دورًا رائدًا ، ويصعب تحديد المناطق شبه الدائرية.
4. قياس الاختلاط الزمني
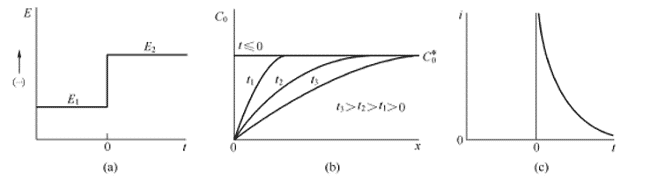
طريقة قياس الزمن هي طريقة تحكم عابرة يمكن استخدامها لتقييم امتصاص وانتشار سطح المحفز. يتم الحصول على منحنى قياس الزمن من خلال تطبيق خطوة محتملة على النظام الكهروكيميائي لقياس تغير إشارة الاستجابة الحالية بمرور الوقت. عندما يتم إعطاء خطوة محتملة ، يظهر الشكل الموجي الأساسي في الشكل 4.1 (أ) ، ويتم تحليل سطح القطب الصلب باستخدام مادة نشطة كهربيًا. بعد تطبيق الخطوة المحتملة ، يتم أولاً تقليل الأنواع النشطة كهربيًا بالقرب من سطح القطب إلى جذري أنيون ثابت ، الأمر الذي يتطلب تيارًا كبيرًا نظرًا لأن العملية تحدث فورًا في لحظة الخطوة. يتم استخدام التيار المتدفق بعد ذلك للحفاظ على الظروف التي يتم فيها تقليل المادة النشطة لسطح القطب بالكامل. يؤدي التخفيض الأولي إلى تدرج تركيز (أي تركيز) بين سطح القطب والمحلول السائب ، وبالتالي تبدأ المادة الفعالة في الانتشار باستمرار نحو السطح وتنتشر في القطب. يتم تقليل المادة الفعالة الموجودة على السطح تمامًا على الفور. يتناسب تدفق الانتشار ، أي التيار ، مع تدرج تركيز سطح القطب. ومع ذلك ، يُلاحظ أنه مع استمرار التفاعل ، تنتشر المادة النشطة في المحلول السائب بشكل مستمر نحو سطح القطب ، مما يتسبب في امتداد منطقة تدرج التركيز تدريجياً نحو المحلول السائب ، وتدرج تركيز السطح للقطب الصلب تدريجيًا يصبح أصغر (مستنفد) ، ويتغير التيار تدريجيًا. صغير. يظهر توزيع التركيز والتيار مقابل الوقت في الشكل 4.1 (ب) والشكل 4.1 (ج).
الشكل 4.1 (أ) يتم تقليل شكل الموجة التجريبية الخطوة ، المتفاعل O عند احتمال E1 ، عند E2 عند سرعة حد الانتشار ؛ (ب) توزيع التركيز في أوقات مختلفة ؛ (ج) منحنى التيار مقابل الوقت
5.تكنولوجيا القطب الكهربائي للقرص
تعد تقنية القطب الكهربائي للقرص الدوار (RDE) مفيدة جدًا في دراسة التفاعل المتجانس المقترن لسطح المحفز ، بحيث يتم إجراء التفاعل الكهروكيميائي على سطح المحفز في حالة مستقرة نسبيًا. يمكن لـ RDE التحكم في المواد ذات الانتشار البطيء ، مثل انتشار الغاز بسهولة في المحلول ، مما يقلل من تأثير طبقة الانتشار على توزيع الكثافة الحالية. وبالتالي ، يتم الحصول على كثافة تيار مستقرة ، والتي تكون في حالة ثابتة تقريبية ، وهو أمر مفيد لعملية التحليل الكهروكيميائي ؛ يمكن لـ RDE التحكم في السرعة التي يصل بها الإلكتروليت إلى سطح القطب عن طريق ضبط سرعة الدوران ، وقياس معلمات عملية التفاعل التحفيزي الكهربي بسرعات دوران مختلفة. التحليلات.
نظرًا لأن البشر أصبحوا أكثر اهتمامًا بتطوير محفزات كهربائية متقدمة لتحويل الطاقة النظيفة ، بالإضافة إلى التأكيد على استخدام بعض الطرق الأساسية لتوصيف تفاعلات التحفيز الكهربي ، هناك حاجة إلى مزيد من الفحص للخطوات الأولية لكل تفاعل لتحديد العناصر المتضمنة. المواد الوسيطة ، وسطح المادة الوسيطة ، وطاقة كل خطوة من خطوات التفاعل الأولية. لا تزال دراسة الطرق الكهروكيميائية تتطلب العديد من التفاصيل حول واجهة الإلكترود والإلكتروليت التي لم تكن معروفة حتى الآن ، مثل الحركية وحواجز التفاعل المتضمنة في الخطوات الأولية الرئيسية لنقل البروتون / الإلكترون ؛ بالقرب من المذيبات والكاتيونات وواجهات التفاعل. وصف الحالة الذرية والجزيئية للأنيون ؛ ولا تزال طرق الحصول على الإشارات في الوقت الفعلي الأسرع والأكثر كفاءة خلال عملية التفاعل الكهروكيميائي في طليعة التفاعلات التحفيزية الكهربية. باختصار ، توفر الدراسة المتعمقة لطرق التوصيف الكهروكيميائي استراتيجية إرشادية لتطوير أنظمة محفز جديدة عالية الكفاءة.