تريد إتقان النقاط الرئيسية للتحليل الحراري وتحليل السعرات الحرارية? راجع هذا المقال يكفي!
التحليل الحراري وتحليل السعرات الحرارية
analysis التحليل الحراري
التحليل الحراري هو فرع مهم من التحليل الآلي ، والذي يلعب دورًا لا غنى عنه في توصيف المادة. بعد فترة طويلة من القرون ، نشأت الحرارة من التحليل الحراري للمعادن والمعادن. في العقود الأخيرة ، كانت علوم البوليمرات وتحليل الأدوية مليئة بالحيوية.
1. التحليل الوزني الحراري
يستخدم تحليل قياس الوزن الحراري (TG أو TGA) للتحكم في كتلة العينة مع درجة الحرارة أو الوقت تحت سيطرة برنامج درجة حرارة معين (أعلى / أسفل / درجة حرارة ثابتة) للحصول على نسبة فقدان الوزن ودرجة حرارة فقدان الوزن. نقطة البداية وقيمة الذروة ونقطة النهاية ...) والمعلومات ذات الصلة مثل مقدار التحلل المتبقي.
يتم استخدام طريقة TG على نطاق واسع في البحث والتطوير وتحسين العملية ومراقبة جودة المواد البلاستيكية والمطاط والطلاء والمستحضرات الصيدلانية والمحفزات والمواد غير العضوية والمواد المعدنية والمواد المركبة. يمكن تحديد الثبات الحراري والاستقرار التأكسدي للمادة تحت أجواء مختلفة. يمكن تحليل العمليات الفيزيائية والكيميائية مثل التحلل ، الامتزاز ، الامتزاز ، الأكسدة والاختزال ، بما في ذلك استخدام نتائج اختبار TG لمزيد من حركية التفاعل الظاهرة. يمكن حساب المادة كميا لتحديد الرطوبة والمكونات المتطايرة والمضافات والمواد المالئة المختلفة.
المبدأ الأساسي لمحلل قياس الثقل الحراري على النحو التالي:
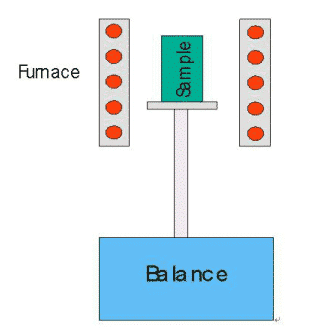
يوضح الشكل أعلاه هيكل محلل قياس الوزن بالحمل العلوي. جسم الفرن هو جسم تسخين ويعمل تحت برنامج درجة حرارة معين. يمكن إخضاع الفرن إلى أجواء ديناميكية مختلفة (مثل N2 و Ar و He وأجواء واقية أخرى و O2 والهواء والأجواء المؤكسدة وغيرها من الأجواء الخاصة ، وما إلى ذلك) ، أو تم إجراء الاختبار تحت فراغ أو جو ثابت. أثناء الاختبار ، يستشعر التوازن عالي الدقة المتصل بالجزء السفلي من حامل العينة الوزن الحالي للعينة في أي وقت ، وينقل البيانات إلى الكمبيوتر. يرسم الكمبيوتر وزن العينة مقابل منحنى درجة الحرارة / الوقت (منحنى TG). عندما يتغير وزن العينة (تشمل الأسباب التحلل ، الأكسدة ، الاختزال ، الامتزاز والامتزاز ، وما إلى ذلك) ، سيظهر كخطوة لفقدان الوزن (أو زيادة الوزن) على منحنى TG ، بحيث يكون فقدان / زيادة الوزن يمكن أن تعرف العملية. منطقة درجة الحرارة التي حدثت وتحديد نسبة الخسارة / الوزن. في حالة إجراء حساب تفاضلي على منحنى TG للحصول على منحنى تفاضلي قياس ثقل حراري (DTG) ، يمكن الحصول على مزيد من المعلومات مثل معدل تغير الوزن.
يظهر منحنى الثقل الحراري النموذجي أدناه:
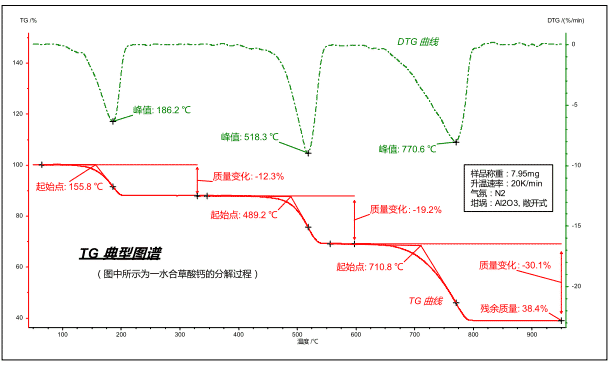
يمكن تحويل الخريطة في إحداثيات درجة الحرارة والوقت.
المنحنى الأحمر: يميز المنحنى الحراري الوزني (TG) وزن العينة كدالة لدرجة الحرارة / الوقت أثناء درجة حرارة البرنامج. الإحداثي هو النسبة المئوية للوزن ، وهي نسبة وزن العينة إلى الوزن الأولي عند درجة الحرارة / الوقت الحالي.
المنحنى الأخضر: منحنى التفاضل الوزني الحراري (DTG) (أي منحنى dm / dt ، منحنى كل نقطة على منحنى TG مقابل إحداثيات الوقت) ، والذي يميز معدل تغير الوزن مع درجة الحرارة / الوقت ، وذروته تتميز النقطة. درجة الحرارة / النقطة الزمنية التي يكون فيها معدل تغير الوزن لكل خطوة من خطوات فقدان / زيادة الوزن هي الأسرع.
بالنسبة لخطوة الخسارة / النمو ، يتم استخدام نقاط الميزة التالية بشكل أكثر شيوعًا:
نقطة انطلاق الاستقراء لمنحنى TG: نقطة التقاطع لخط المماس عند المستوى قبل خطوة TG ونقطة المماس عند نقطة انعطاف المنحنى يمكن استخدامها كنقطة درجة حرارة مرجعية يتم عندها عملية فقدان / زيادة الوزن يبدأ ، ويستخدم في الغالب لوصف الاستقرار الحراري للمادة.
نقطة إنهاء استقراء منحنى TG: يمكن استخدام نقطة تقاطع خط المماس عند المستوى بعد خطوة TG ونقطة المماس عند نقطة انعطاف المنحنى كنقطة درجة حرارة مرجعية في نهاية عملية فقدان / زيادة الوزن.
ذروة منحنى DTG: درجة الحرارة / النقطة الزمنية التي يكون فيها معدل تغير الكتلة هو الأكبر ، وهو ما يقابل نقطة الانعطاف على منحنى TG.
تغيير الكتلة: تحليل فرق الكتلة بين أي نقطتين على منحنى TG لتمثيل التغيير الشامل للعينة الناجم عن خطوة فقدان الوزن (أو زيادة الوزن).
الكتلة المتبقية: الكتلة المتبقية في العينة في نهاية القياس.
بالإضافة إلى ذلك ، في البرنامج ، نقطة الانحناء لمنحنى TG (ما يعادل درجة حرارة ذروة DTG) ، ونقطة انطلاق استقراء منحنى DTG (أقرب إلى درجة حرارة بدء التفاعل الحقيقي) ، ونقطة إنهاء استقراء منحنى DTG (أقرب إلى الخاصية المميزة يتم تمييز معلمات مثل درجة حرارة نهاية التفاعل بالمعنى الحقيقي.
2. تحليل القياسات
Calorimetry هو نظام يدرس كيفية قياس التغيرات في الحرارة المصاحبة للعمليات المختلفة. يمكن من حيث المبدأ الحصول على بيانات الخصائص الحرارية الدقيقة من خلال تجارب قياس السعرات الحرارية ، التي يتم إجراؤها بواسطة أجهزة قياس السعرات الحرارية.
التحليل الحراري التفاضلي (DTA) هو طريقة تحليل حراري تقيس فرق درجة الحرارة بين عينة ومرجع عند درجة حرارة مبرمجة. المسح الحراري التفاضلي (DSC) هو طريقة تحليل حراري تقيس العلاقة بين فرق الطاقة ومدخلات درجة الحرارة للعينة والمرجع تحت ظروف درجة الحرارة المبرمجة. تختلف المعاني المادية للطريقتين. يمكن لـ DTA اختبار النقاط المميزة لدرجة الحرارة فقط مثل درجة حرارة المرحلة الانتقالية. لا يمكن لـ DSC قياس درجة حرارة تغير الطور فقط ، ولكن أيضًا قياس تغير الحرارة أثناء تغيير الطور. الذروة الطاردة للحرارة والذروة الماصة للحرارة على منحنى DTA ليس لها معنى مادي محدد ، في حين أن الذروة الطاردة للحرارة والذروة الماصة للحرارة على منحنى DSC تمثل إطلاق الحرارة وامتصاص الحرارة ، على التوالي. لذلك ، نستخدم DSC كمثال لتحليل تحليل السعرات الحرارية.
القياس التفاضلي للمسح الضوئي (DSC) هو مراقبة تغير فرق طاقة تدفق الحرارة بين نهاية العينة والنهاية المرجعية مع درجة الحرارة أو الوقت تحت سيطرة برنامج درجة حرارة معينة (أعلى / أسفل / درجة حرارة ثابتة). بهذه الطريقة ، يتم حساب معلومات التأثير الحراري للعينة أثناء برنامج درجة الحرارة ، مثل ماص للحرارة ، وطارد للحرارة ، وتغير نوعي للحرارة ، وما إلى ذلك ، وامتصاص الحرارة (المحتوى الحراري الحراري) ودرجة الحرارة المميزة (نقطة البداية ، قيمة الذروة ، نقطة النهاية…) للتأثير الحراري.
تستخدم طريقة DSC على نطاق واسع في مختلف المجالات مثل البلاستيك والمطاط والألياف والطلاءات والمواد اللاصقة والأدوية والأغذية والكائنات البيولوجية والمواد غير العضوية والمواد المعدنية والمواد المركبة. يمكنه دراسة عملية انصهار وتبلور المواد ، وانتقال الزجاج ، وانتقال الطور ، وانتقال البلورات السائلة ، والتصلب ، وثبات الأكسدة ، ودرجة حرارة التفاعل ومحتوى التفاعل ، ويتم قياس حرارة ونقاء المادة المحددة ، وتوافق كل مكون من مكونات يتم دراسة الخليط ، ويتم حساب معلمات التبلور والتفاعل الحركي.
المبدأ الأساسي لمقياس السعرات الحرارية للمسح التفاضلي هو كما يلي:
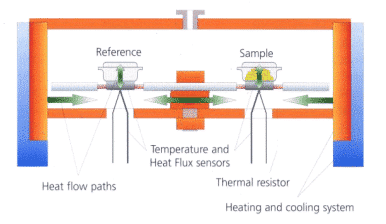
كما هو موضح في الشكل أعلاه ، فإن العينة معبأة بعينة وتوضع على قرص المستشعر مع بوتقة مرجعية (عادة فارغة). يتم الاحتفاظ بالاثنين متماثلًا حراريًا وفي فرن موحد وفقًا لبرنامج درجة حرارة معين (التسخين الخطي) ، تم اختبار التبريد ، ودرجة الحرارة الثابتة ، ومجموعات منها) واستخدم زوج من المزدوجات الحرارية (المزدوجة الحرارية المرجعية ، عينة الحرارية المزدوجة) لقياس مستمر فرق درجة الحرارة بين الاثنين. نظرًا لأن جسم الفرن لأخذ عينة من عملية التسخين / المرجعية يفي بمعادلة التوصيل الحراري فورييه ، فإن فرق تدفق حرارة التسخين عند كلا الطرفين يتناسب مع إشارة فرق درجة الحرارة ، لذلك يمكن تحويل إشارة فرق درجة الحرارة الأصلية إلى إشارة فرق تدفق الحرارة عن طريق الحرارة تصحيح التدفق ، والوقت / درجة الحرارة عبارة عن تعيين مستمر للحصول على خريطة DSC.
يتسبب التأثير الحراري للعينة في عدم توازن التدفق الحراري بين المرجع والعينة. نظرًا لوجود المقاومة الحرارية ، يتناسب فرق درجة الحرارة بين المرجع والعينة () مع فرق تدفق الحرارة. سيتم دمج الوقت للحصول على الحرارة: (درجة الحرارة ، المقاومة الحرارية ، خصائص المواد ...)
نظرًا للتناظر الحراري بين المحتوىين الحراريين ، فإن فرق الإشارة بين النهاية المرجعية ونهاية العينة يقترب من الصفر في غياب التأثيرات الحرارية في العينة. يتم الحصول على خط أفقي تقريبي على الخريطة ، يسمى "خط الأساس". بالطبع ، من المستحيل على أي أداة فعلية تحقيق التماثل الحراري المثالي. بالإضافة إلى ذلك ، لا يكون الفرق في السعة الحرارية بين نهاية العينة والنهاية المرجعية أفقيًا تمامًا ، وهناك تموج معين. يسمى هذا فولت عادة "انجراف خط الأساس".
عندما يكون للعينة تأثير حراري ، يتم إنشاء فرق معين في درجة الحرارة / فرق إشارة تدفق الحرارة بين نهاية العينة والنهاية المرجعية. من خلال التآمر المستمر لفرق الإشارة مقابل الوقت / درجة الحرارة ، يمكن الحصول على خريطة مشابهة لما يلي:
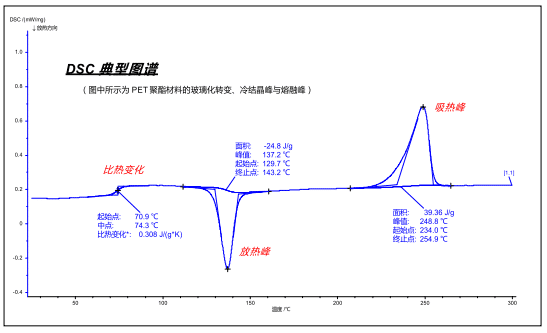
وفقًا لمعيار DIN واللوائح الديناميكية الحرارية ، فإن الارتفاع (القيمة الموجبة) الموضح في الشكل هو الذروة الماصة للحرارة للعينة (التأثير الماص للحرارة النموذجي هو الذوبان ، التحلل ، الامتزاز ، وما إلى ذلك) ، والأسفل (القيمة السلبية) هي الذروة الطاردة للحرارة (التأثير الطارد للحرارة النموذجي هو التبلور ، الأكسدة ، التصلب ، وما إلى ذلك ، وينعكس تغير الحرارة المحدد في تغيير ارتفاع خط الأساس ، أي انعطاف شبيه بالخطوة على المنحنى (التغير الحراري النموذجي المحدد التأثير هو التزجج ، الانتقال المغنطيسي ، وما إلى ذلك)).
يمكن تحويل الخريطة في إحداثيات درجة الحرارة والوقت.
بالنسبة للامتصاص / الذروة الطاردة للحرارة ، يمكن تحليل نقطة البداية وقيمة الذروة ونقطة النهاية ومنطقة الذروة بشكل أكثر شيوعًا. بعض من:
نقطة البداية: النقطة التي يكون عندها خط الأساس قبل الذروة مماسًا للمماس عند نقطة الانعطاف على يسار القمة ، غالبًا ما يُستخدم لتمييز درجة الحرارة (الوقت) التي يبدأ عندها التأثير الحراري (التفاعل الفيزيائي أو الكيميائي) تحدث.
الذروة: درجة الحرارة (الوقت) التي يكون عندها أقصى تأثير امتصاص / طارد للحرارة.
نقطة الإنهاء: النقطة التي يكون عندها خط الأساس بعد الذروة مماسًا إلى المماس على يمين القمة ، والذي يتوافق مع نقطة البداية وغالبًا ما يُستخدم لتمييز درجة الحرارة (الوقت) التي يكون فيها التأثير الحراري (الفيزيائي أو الكيميائي) رد فعل) ينتهي.
المساحة: المنطقة التي تم الحصول عليها عن طريق دمج قمم الامتصاص / الطاردة للحرارة ، في J / g ، لتوصيف كمية الحرارة التي يتم امتصاصها / تصريفها بواسطة وحدة وزن العينة أثناء عملية فيزيائية / كيميائية.
بالإضافة إلى ذلك ، يمكن الإشارة إلى المعلمات المميزة مثل الارتفاع والعرض والمنحنى المتكامل لمنطقة الذروة الممتصة / الطاردة للحرارة في البرنامج. لعملية تغيير الحرارة المحددة ، يمكن تحليل المعلمات مثل نقطة البداية ، نقطة المنتصف ، نقطة النهاية ، نقطة الانعطاف ، وقيمة تغير الحرارة المحددة.
Ⅱ. معدات التحليل الحراري
1. محلل قياس الوزان الحراري
تتميز أداة TG الحديثة ببنية معقدة. بالإضافة إلى فرن التسخين الأساسي والتوازن عالي الدقة ، هناك أجزاء تحكم إلكترونية ، وبرمجيات ، وسلسلة من المعدات المساعدة. يظهر هيكل Netzsch TG209F3 في الشكل أدناه:
يمكن رؤية الغاز الواقي وغاز التطهير في الشكل. عادة ما يكون الغاز الواقي خاملًا لـ N2. يتم تمريره إلى الفرن من خلال غرفة الوزن ومنطقة توصيل المفصل ، بحيث يمكن وضع التوازن. بيئة عمل مستقرة وجافة تمنع الرطوبة ، والحمل الحراري للهواء ، وتحلل عينات الملوثات من التأثير على التوازن. يسمح الجهاز بتوصيل نوعين مختلفين من غازات التطهير (purge1 و purge2) في نفس الوقت ويتم التبديل أو الخلط تلقائيًا أثناء القياس حسب الحاجة. الاتصال الشائع هو الاتصال الذي يتم فيه توصيل N2 كجو تطهير خامل للتطبيقات التقليدية ؛ والآخر مرتبط بالهواء كجو مؤكسد. من حيث إكسسوارات التحكم في الغاز ، يمكن تجهيزه بمقياس دوار تقليدي ، صمام الملف اللولبي ، أو مقياس تدفق الكتلة (MFC) بدقة وأتمتة أعلى.
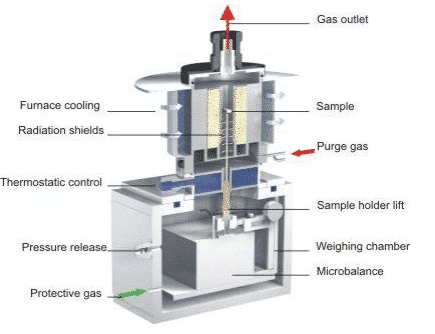
يقع مخرج الغاز في الجزء العلوي من الجهاز ويمكن استخدامه لتفريغ الغاز الحامل والمنتجات الغازية في الغلاف الجوي. كما يمكن توصيله بأنظمة FTIR و QMS و GC-MS وأنظمة أخرى باستخدام خط نقل ساخن لتوصيل غازات المنتج لهذه الأجهزة. كشف المكون. يجعل هيكل التحميل العلوي للجهاز وتصميم مسار الغاز الطبيعي الناعم معدل تدفق الغاز الحامل صغيرًا ، وتركيز غاز المنتج مرتفعًا ، وتباطؤ الإشارة ، وهو أمر مفيد جدًا للدمج مع هذه الأنظمة للتحليل الفعال لل مكونات الغاز المتطور.
تم تجهيز الجهاز بجهاز تحكم حراري لعزل الفرن من جزئين من الميزان ، والذي يمكن أن يمنع بشكل فعال نقل الحرارة إلى وحدة التوازن عندما يكون الفرن في درجة حرارة عالية. بالإضافة إلى ذلك ، فإن التطهير المستمر من أعلى إلى أسفل لغاز الحماية يمنع نقل الحرارة الناجم عن الحمل الحراري للهواء الساخن ، وتعزل الدروع الإشعاعية حول حامل العينة عوامل الإشعاع الحراري في بيئة درجة حرارة عالية. تضمن المقاييس أن الميزان عالي الدقة في بيئة درجة حرارة مستقرة ولا يتداخل مع منطقة درجة الحرارة العالية ، مما يضمن استقرار إشارة قياس الثقل الحراري.
2. المسعر التفاضلي المسح
تعد أدوات DSC الحديثة أكثر تعقيدًا في الهيكل ، بالإضافة إلى فرن التسخين الأساسي وأجهزة الاستشعار ، بالإضافة إلى أجزاء التحكم الإلكترونية والبرمجيات ومجموعة من المعدات المساعدة. يوضح الرسم البياني أدناه هيكل Netzsch DSC204F1:
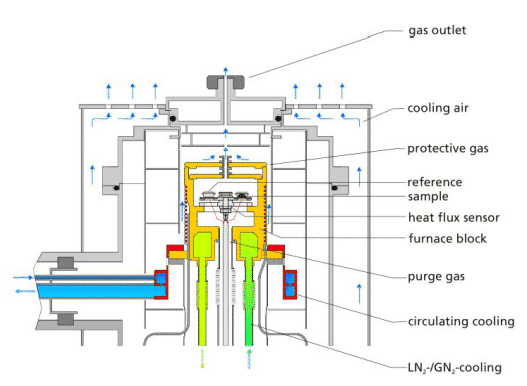
يمكن رؤية الغاز الواقي وغاز التطهير في الشكل. عادة ما يتم تمرير الغاز الواقي عبر محيط الفرن باستخدام N2 الخامل ، والذي يمكن أن يحمي جسم التسخين ، ويطيل عمر الخدمة ، ويمنع جسم الفرن. تأثير التجمد على المحيط عند درجات حرارة منخفضة. تسمح الأداة بتوصيل نوعين مختلفين من غازات التطهير في وقت واحد وتبديلها أو خلطها تلقائيًا أثناء القياس حسب الحاجة. الاتصال التقليدي هو الاتصال الذي يتم فيه توصيل N2 كجو تطهير خامل للتطبيقات التقليدية ؛ والآخر متصل بالهواء أو O2 لاستخدامه في جو مؤكسد. من حيث إكسسوارات التحكم في الغاز ، يمكن تجهيزه بمقياس دوار تقليدي ، صمام الملف اللولبي ، أو مقياس تدفق الكتلة (MFC) بدقة وأتمتة أعلى.
يمكن توصيل الجهاز بثلاثة أنواع مختلفة من معدات التبريد. واحد هو نظام النيتروجين السائل LN2 / GN2 التبريد) ، أحدهما يدور التبريد أو المبرد الداخلي ، والآخر هو تبريد الهواء. تتميز طرق التبريد الثلاثة هذه بخصائص مختلفة وتطبيقات مناسبة. الهواء المضغوط بسيط نسبيًا ، ودرجة حرارة التبريد الدنيا هي درجة الحرارة العادية ، ومناسبة للمناسبات التي لا تتطلب تطبيقات درجة حرارة منخفضة (مثل البلاستيك ، صناعة الراتنج بالحرارة ، وما إلى ذلك) ، وغالبًا ما تستخدم للتبريد التلقائي بعد نهاية القياس ، بحيث يتم تبريد جسم الفرن إلى درجة الحرارة العادية ، من السهل إضافة العينة التالية ؛ يتميز نظام النيتروجين السائل بتبريد وخفض أسرع إلى درجة حرارة أقل (-180 درجة مئوية) من التبريد الميكانيكي. العيب هو أن النيتروجين السائل نفسه قابل للاستهلاك. تحتاج إلى إضافة ، هناك عوامل تكلفة المواد الاستهلاكية ؛ في حين أن التبريد الميكانيكي أدنى من النيتروجين السائل في معدل التبريد والحد من درجة الحرارة ، ولكن في الأساس ، لا يمكن استخدام أي عوامل قابلة للاستهلاك طوال الوقت ، وهو ما يفيده.
العوامل التجريبية المؤثرة على التحليل والقياس الحراري
1. تأثير معدل التسخين على نتائج تجارب التحليل الحراري
لمعدل ارتفاع درجة الحرارة تأثير كبير على نتائج تجربة التحليل الحراري. بشكل عام ، يمكن تلخيصها على النحو التالي.
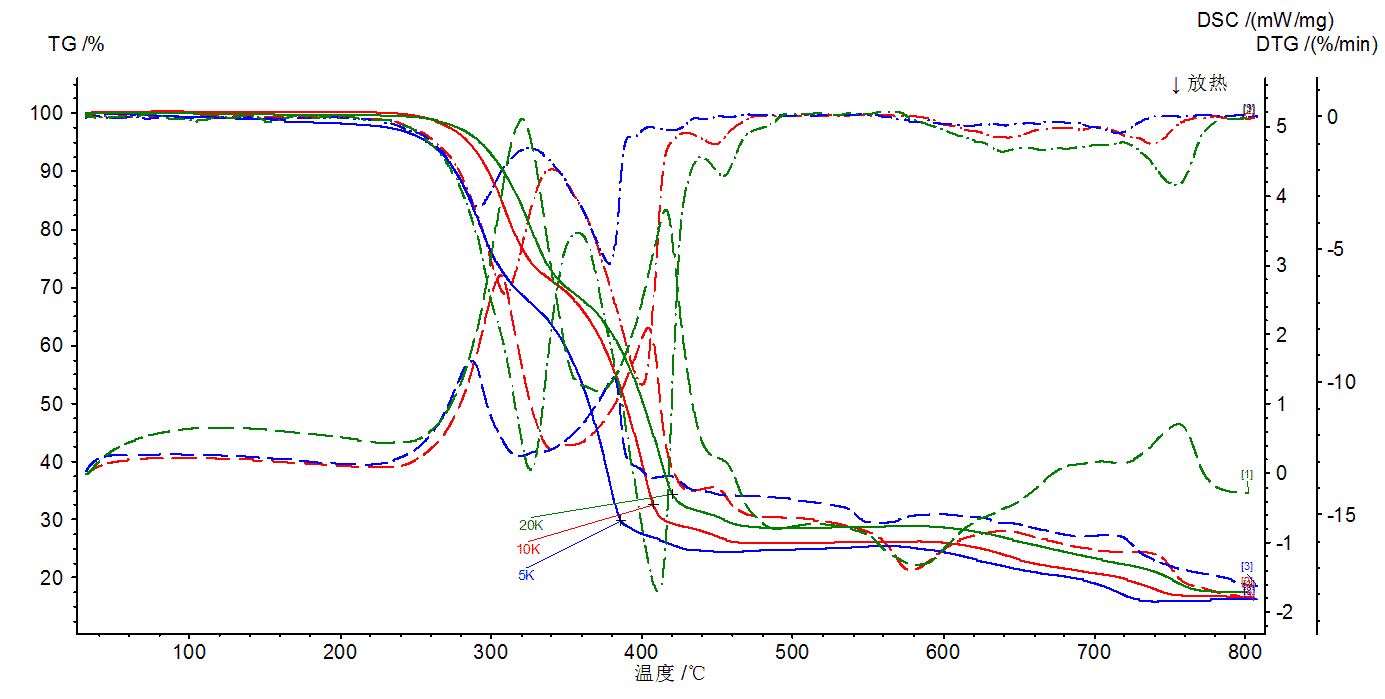
(1) بالنسبة لتفاعل معين للعينة ممثلة بمنحنى TG ، DSC ، عادة ما تكون الزيادة في معدل زيادة درجة الحرارة بحيث تزيد درجة الحرارة الأولية للتفاعل Ti ، وذروة درجة الحرارة Tp ، ودرجة حرارة الإنهاء Tf. ارتفاع سريع في درجة الحرارة ، بحيث لا يكون التفاعل قادرًا على المتابعة حتى الآن ، فإنه يدخل إلى درجة حرارة أعلى ، وتأخر تفاعل التجميع (في الصورة أعلاه).
(2) ارتفاع درجة الحرارة السريع هو دفع التفاعل إلى سرعة أعلى في منطقة درجة حرارة عالية ، أي ليس فقط ذروة درجة الحرارة Tp لمنحنى DSC ، ولكن أيضًا يتم تضييق اتساع الذروة وذروته (كما هو موضح في الرقم أعلاه).
2. تأثير جرعة العينة وحجم الجسيمات على تجارب التحليل الحراري
تفيد كمية صغيرة من العينة في انتشار منتج الغاز ودرجة الحرارة الداخلية للعينة ، مما يقلل من درجة حرارة التدرج ويقلل من انحراف درجة حرارة العينة عن ارتفاع درجة الحرارة الخطية في البيئة ، والذي ينتج عن الامتصاص و آثار إطلاق الحرارة للعينة. أظهرت التجارب أن منطقة الذروة لا تزال مرتبطة بحجم جسيم العينة. كلما كان الجسيم أصغر ، زادت مساحة الذروة الطاردة للحرارة لمنحنى DSC. بالإضافة إلى ذلك ، هناك فجوة بين جزيئات العينة المتراصة المتراكمة ، مما يجعل العينة متدهورة حرارياً ، وكلما كانت الجسيمات أصغر ، كلما كان من الممكن تكديس الأكوام وتوصيل الحرارة جيدًا. بغض النظر عن حجم الجسيمات في العينة ، ليس من السهل تكرار كثافة البطريق وستؤثر أيضًا على تضاريس منحنى TG.
3. تأثير الغلاف الجوي على نتائج تجارب التحليل الحراري
من أجل التفاعل لتكوين منتج غازي ، إذا لم تتم إزالة منتج الغاز في الوقت المناسب ، أو زاد الضغط الجزئي للمنتج الغازي في الغلاف الجوي بوسائل أخرى ، يتم نقل التفاعل إلى درجة حرارة عالية. الموصلية الحرارية للغلاف الجوي جيدة ، وهو مفيد لتوفير المزيد من الحرارة للنظام وزيادة معدل تفاعل التحلل. تتزايد العلاقة بين الموصلية الحرارية لثلاثة غازات خاملة من الأرجون والنيتروجين والهليوم ودرجة الحرارة في التسلسل.
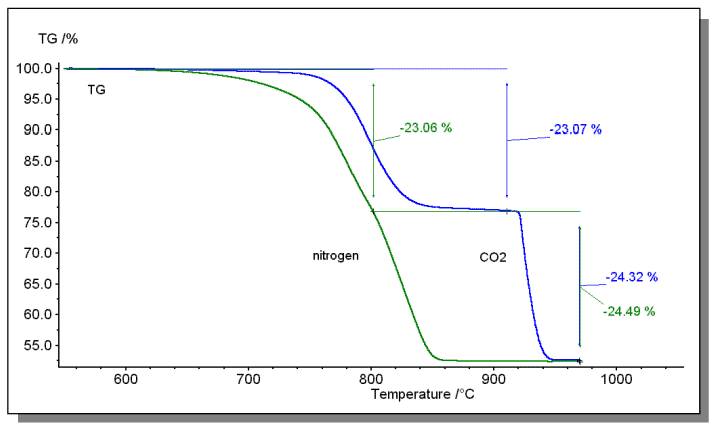
يوضح الشكل أدناه اختبار التحلل من الدولوميت. تتكون عملية التحلل من الخطوتين التاليتين:
MgCO3 → MgO + CO2 ↑
CaCO3 → CaO + CO2 ↑
في حالة تطهير N2 التقليدي ، تكون درجة حرارة خطوتين التحلل متشابهة ، وتأثير الفصل ليس جيدًا. من الصعب حساب محتوى مكوني MgCO3 و CaCO3 بدقة. لذلك ، تم استخدام ثاني أكسيد الكربون كجو تطهير في هذا المثال. نظرًا لأن كلتا خطوات إنقاص الوزن تولد ثاني أكسيد الكربون ، فإن استخدام ثاني أكسيد الكربون كغلاف جوي للتطهير سيؤثر على التوازن الكيميائي ويسبب رد الفعل على "التأخير" (لا تتأثر نسبة فقدان الوزن). نظرًا لأن "درجة التأخير" للتحلل المكون من خطوتين ليست هي نفسها ، فإن تأخير المرحلة الثانية من فقدان الوزن (تحلل كربونات الكالسيوم CaCO3) يكون أكثر أهمية. بهذه الطريقة ، يتم تحقيق تأثير الفصل التدريجي بشكل فعال ، ويمكن حساب نسبة كتلة MgCO3 في العينة بدقة لتكون 44.0% (MgCO3 / CO2 = 1.91) ، ونسبة كتلة CaCO3 هي 55.3% (CaCO3 / ثاني أكسيد الكربون = 2.27).
4. تأثير الطفو والحمل الحراري والاضطراب على منحنى TG
تنخفض كثافة الطور الغازي للمساحة المتوسطة في حامل العينة مع زيادة درجة الحرارة ، وبالتالي ينخفض الطفو ، والذي يتم التعبير عنه على أنه زيادة واضحة في الوزن. بالنسبة لحاوية العينة ، يتسبب الهواء المتدفق لأعلى في فقدان الوزن الواضح ، ويتسبب الاضطرابان الهوائيان في زيادة الوزن ، وهو ما يرتبط بحجم وشكل البوتقة ، والتي يمكن تعديلها عن طريق مخرج الهواء فوق حاوية العينة ، لكن منحنى TG مصنوع. من الصعب ألا يكون هناك تغير كتلة واضح على مدى درجة الحرارة بالكامل.
5. أثر ضيق العينة على النتائج التجريبية
تؤثر درجة ضيق العينة المحمل في البوتقة على انتشار منتج غاز الانحلال الحراري في الهواء المتوسط المحيط واتصال العينة مع الغلاف الجوي. على سبيل المثال ، تفقد الخطوة الثانية من مونوهيدرات أكسالات الكالسيوم CaC2O4 · H2O تفاعل أول أكسيد الكربون CO: CaC2O4 · H2O → CaCO3 + CO ↑
عندما يكون الوسط هو الهواء ، إذا كانت العينة فضفاضة وذات جو مؤكسد كافٍ ، فإن منحنى DSC له تأثير طارد للحرارة (ذروة درجة الحرارة 511 درجة مئوية) ، وهو أكسدة CO: 2CO + O2 → 2CO2 ، إذا كانت العينة نسبيًا مدمج ، إنه في حالة الغياب في حالة الأكسجين ، يكون لمنحنى DSC تأثير ماص للحرارة. انظر أدناه.
فضفاض (1) وأكثر امتلاء (2)
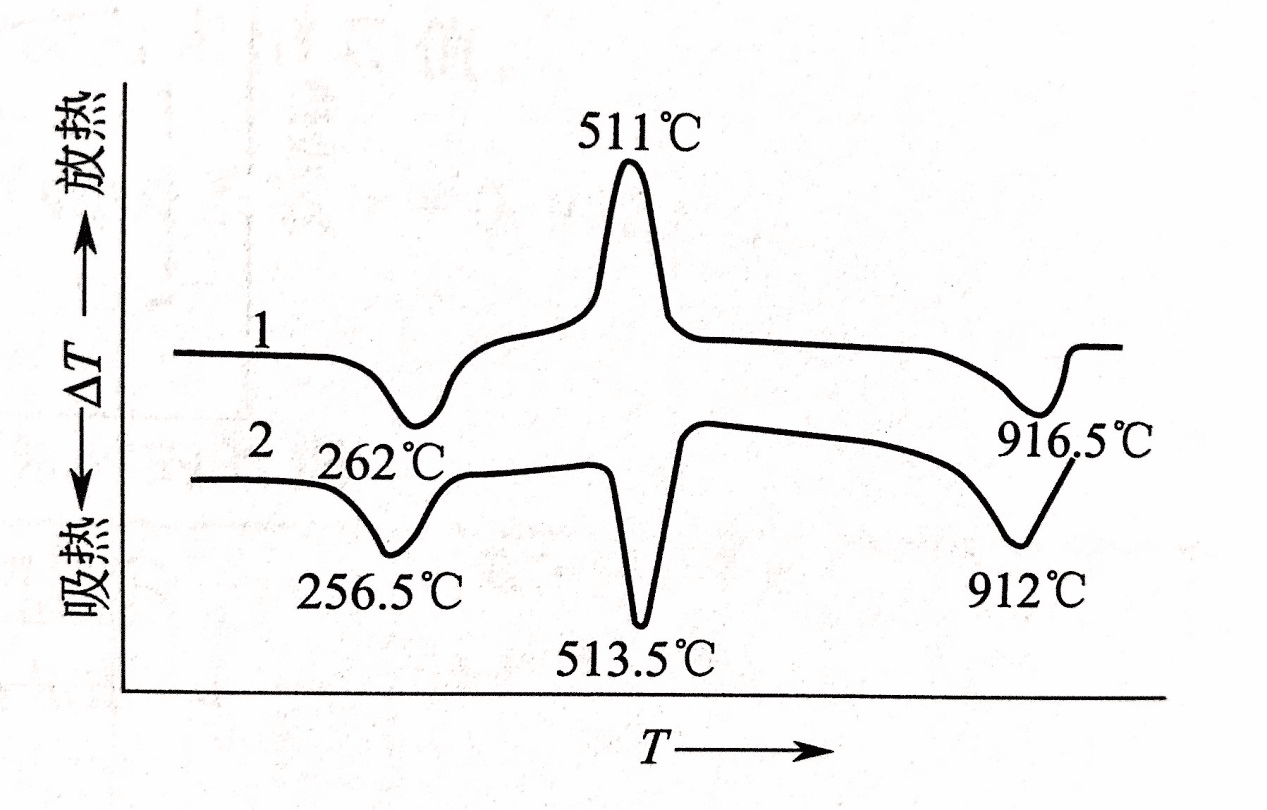
Ⅳ قياس التحولات المختلفة بتقنية التحليل الحراري
1. قياس التزجج
بالنسبة للمواد الصلبة غير المتبلورة ، يحدث التزجج أثناء التسخين ، من المواد الصلبة غير المتبلرة إلى ديناميكيات التدفق (مرونة عالية للمواد البوليمرية). في هذه العملية ، إلى جانب تغيير الحرارة المحددة ، ينعكس في منحنى DSC كخطوة باتجاه اتجاه امتصاص الحرارة.
لديها. من هذا التحليل ، يمكن الحصول على درجة حرارة التزجج للمادة.
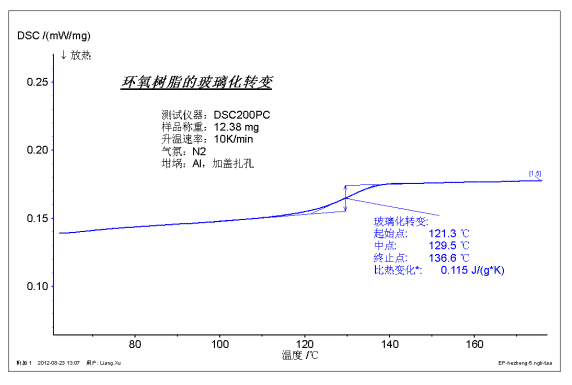
يوضح الشكل أعلاه اختبار التزجج لعينة من راتنجات الايبوكسي. وفقًا للمعايير الدولية ، يأخذ التزجج بشكل عام نقطة المنتصف ، وهي 129.5 درجة مئوية. يميز تغير الحرارة المحدد تقريبًا شدة الانتقال.
2. قياس التبلور والصهر
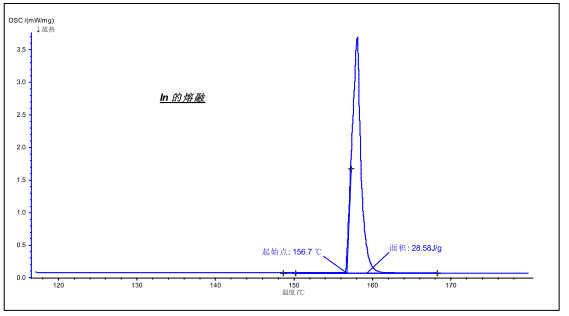
انصهار البلورة عبارة عن مرحلة انتقالية من الدرجة الأولى مصحوبة بتأثير ماص للحرارة أثناء عملية الصهر. باستخدام DSC ، يمكن قياس التأثير الماص للحرارة للحصول على معلومات مثل نقطة الانصهار ، وانصهار المحتوى الحراري ، وما شابه.
يوضح الشكل أعلاه ذوبان المعدن في. نقطة الانصهار هي 156.7 درجة مئوية (النظري 156.6 درجة مئوية) ، المحتوى الحراري هو 28.58 جول / جرام (القيمة النظرية 28.6 جول / جرام).
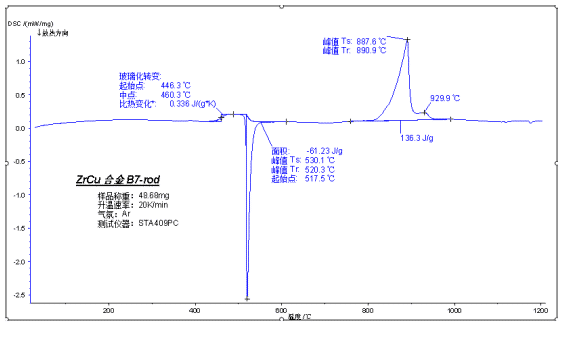
يوضح الشكل أعلاه التزجج والتبلور البارد واختبار انصهار السبائك غير المتبلورة أثناء التسخين. تحتوي السبائك غير المتبلورة على درجة عالية من الطور غير المتبلور بسبب عدم التبلور الكافي في درجة حرارة الغرفة ، لذلك هناك انتقال زجاجي كبير أثناء التسخين. ثم تظهر ذروة بلورة باردة ، وتحتوي ذروة الذوبان النهائية على الذوبان المتزامن للبلورة في درجة حرارة الغرفة والجزء البلوري المضاف لعملية البلورة الباردة.
خامسا - التحليل النموذجي للتحليل الحراري
1. الاستقرار الحراري
باستخدام محلل قياس الثقل الحراري ، من خلال تحليل المرحلة الأولية من عملية التحلل ، من السهل فهم الاستقرار الحراري للمادة والحصول على معلومات حول الحد الأعلى لدرجة حرارة الاستخدام.
من أجل شرح درجة الحرارة التي يمكن أن تمثل الاستقرار الحراري ، يمكن استخدام طريقة نقطة البداية الخارجية التقليدية (يمكن استخدام خطوة TG أو ذروة DTG كنقطة انطلاق خارجية) ، ولكن درجة الحرارة تخضع لشرط حدود التحليل (خذ نطاق المماس) التأثير ، في بعض الأحيان غير مستقر بما فيه الكفاية. في المجال الصناعي ومناسبات مراقبة الجودة ، يتم استخدام أكثر من 1% و 2% و 5% لفقدان الوزن لوصف الاستقرار الحراري للمنتج ، وتكون نتيجة الحساب أكثر دقة وموثوقية.
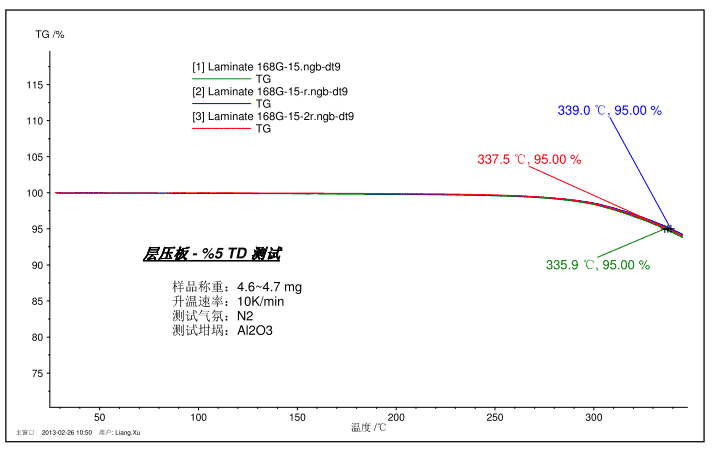
يوضح الشكل أعلاه طيف اختبار قدره 5% TD (فقدان الوزن 5%) لعينة صفائحية كمادة ثنائي الفينيل متعدد الكلور. تم اختبار العينة ثلاث مرات في المجموع ، وكانت قابلية التكاثر جيدة ، وكان 5% TD في نطاق 337.5 ± 1.5 درجة مئوية.
2. عملية Pyrolysi
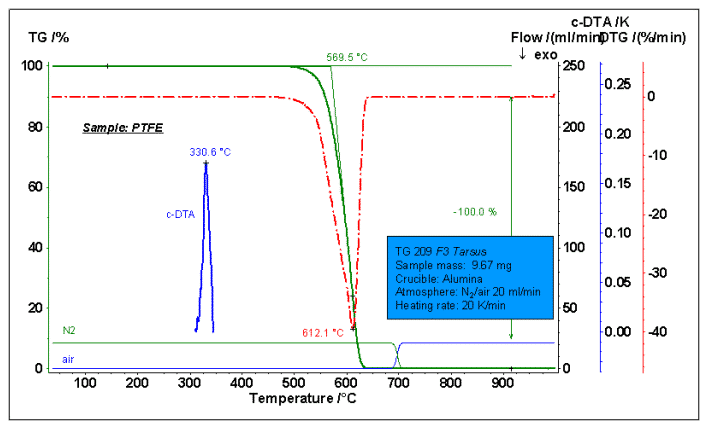
يوضح الشكل أعلاه اختبار عملية التحلل الحراري لـ polytetrafluoroethylene PTFE. تم استخدام الغلاف الجوي N2 قبل 700 درجة مئوية ، وتم تحويله إلى الهواء بعد 700 درجة مئوية. PTFE هي مادة مقاومة لدرجة الحرارة العالية ، ودرجة حرارة التحلل الأولي تصل إلى 500 درجة مئوية أو أعلى (نقطة بداية القطع الخارجي TG هي 569.5 درجة مئوية في الشكل) ، ونقطة فقدان الوزن القصوى (درجة حرارة الذروة DTG) هي 612.1 درجة مئوية. كانت العينة 100% فقدان الوزن تمامًا تحت جو خامل ولم يتم تكوين بقايا كربون. يمكن التحقق من ذلك عن طريق التبديل من الرسم البياني إلى الهواء دون مزيد من فقدان الوزن. بالإضافة إلى ذلك ، يعطي منحنى c-DTA ذوبان ذروة PTFE عند درجة حرارة 330.6 درجة مئوية.
3. تحليل المكونات
باستخدام محلل قياس الثقل الحراري ، يمكن حساب نسبة المكون الداخلي للعديد من المواد بناءً على نتائج قياس فقدان الوزن متعدد المراحل باستخدام معدل تسخين مناسب وجو قياس ، وترتيب التبديل بين الأجواء المختلفة بشكل منطقي.
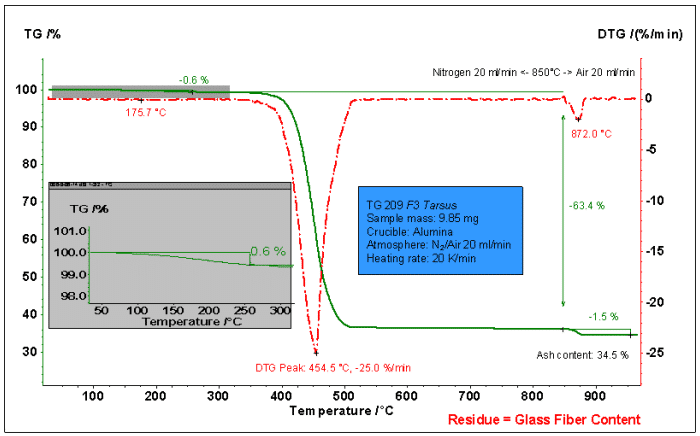
يوضح الشكل أعلاه تحليل عملية فقدان الوزن من الألياف الزجاجية المقواة PA66. استخدم N2 قبل 850 درجة مئوية ، وانتقل إلى الهواء بعد 850 درجة مئوية. يتبين من الشكل أن فقدان الوزن ينقسم إلى المراحل التالية:
1. كمية صغيرة من فقدان الوزن قبل 1.300 درجة مئوية: فقدان الوزن 0.6%. قد تكون الرطوبة الممتزة في المادة وبعض المواد المتطايرة العضوية.
2. 300 ~ 850 درجة مئوية: خطوة فقدان الوزن الرئيسية ، فقدان الوزن هو 63.4%. تحلل PA66.
3. بعد التبديل إلى الهواء عند 850 درجة مئوية: يكون فقدان الوزن 1.5% ، وهو ما يتوافق مع فقدان حرارة الكربون (منتج التحلل PA66).
الجودة المتبقية: 34.5%. يجب أن يكون مكونًا من ألياف زجاجية لا تتحلل أو تتأكسد.
من التحليل أعلاه ، يمكن حساب نسبة PA66 في العينة لتكون 64.9% (63.4 + 1.5). نسبة الألياف الزجاجية هي 34.5%. كان الجزء المتبقي من الرطوبة / المتطايرة 0.6%.
4. التسامي المتطاير
باستخدام محلل قياس الوزان الحراري ، يمكن اختبار عملية التطاير لجيل من العينات (مثل زيت التشحيم) وتميز استقرارها.
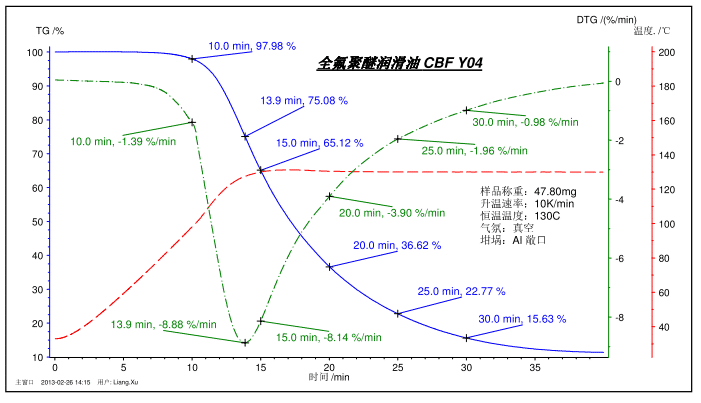
يوضح الشكل أعلاه اختبار عملية التطاير لزيوت التشحيم. تم رفع برنامج درجة الحرارة من درجة حرارة الغرفة إلى 130 درجة مئوية وحفظها في درجة حرارة ثابتة. يوضح الشكل النسبة المئوية للكتلة عند 10 ، 15 ، 20 ، 25 ، 30 دقيقة ، وأسرع فقدان للتركيز عند 13.9 دقيقة ، ومعدل فقدان الوزن DTG المقابل. وبالمثل ، يمكن لـ TG أيضًا قياس عملية التطاير (التسامي) لبعض العينات الصلبة ، مثل الكافور ، لتمييز استقرار التخزين.
5. الامتزاز والامتزاز
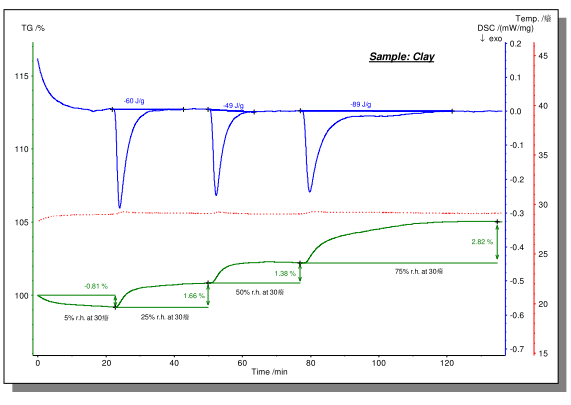
يوضح الشكل أعلاه عملية الجفاف وامتصاص الماء للطين المختبر على جهاز STA تحت أجواء رطوبة مختلفة. تم إجراء الاختبار عند درجة حرارة ثابتة تبلغ حوالي 30 درجة مئوية باستخدام مولد الرطوبة لخلق جو تطهير رطوبة معينة. يمكن ملاحظة أنه في ظل جو نقي أكثر جفافاً من 5% رطوبة نسبية ، أظهرت العينة عملية تجفيف مع فقدان وزن قدره 0.81%. عندما تم تحويل الغلاف الجوي إلى 25% رطوبة نسبية ، أظهرت العينة امتصاص الماء مع زيادة الوزن 1.66%. بعد الرطوبة النسبية 50% و 75% ، تمتص كل العينات الماء ، وكان اكتساب الوزن 1.38% و 2.82% على التوالي. في نفس الوقت ، على منحنى DSC الأزرق ، يمكن ملاحظة التأثير الطارد للحرارة و المحتوى الحراري لعملية امتصاص الماء.
6. تأثير معدل التبريد على التبلور
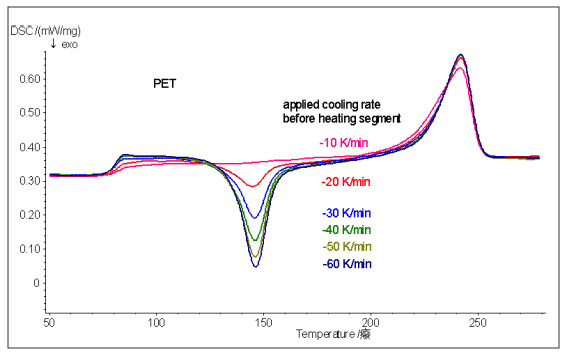
يقارن الشكل أعلاه النتائج التي تم الحصول عليها بارتفاع درجة حرارة ثانية أخرى بعد تبريد عينة أخرى من PET من الحالة المنصهرة إلى درجة حرارة عادية باستخدام معدل تبريد مختلف. يمكن ملاحظة أنه كلما كان معدل التبريد أسرع ، كلما قل تبلور العينة ، وكلما زادت مساحة ذروة التبلور البارد التي تم الحصول عليها بالتسخين الثاني ، كلما انخفضت التبلور.
سيؤثر التبلور المختلف على الخواص الميكانيكية للمادة (المرونة ، الليونة ، مقاومة الصدمات ، إلخ) ، الخواص البصرية ، مقاومة المذيبات ، وقابلية المعالجة. لذلك ، في عملية إنتاج اللدائن الحرارية ، تعد التبلور أيضًا مؤشرًا مهمًا للكشف والتحكم.
7. استقرار الأكسدة
يمكن اختبار الثبات التأكسدي للمادة باستخدام DSC. تتضمن طرق الاختبار المحددة طريقة OIT ، وطريقة أكسدة درجة الحرارة الديناميكية.
فترة تحريض الأكسدة (OIT) هي طريقة اختبار قياسية لصناعة البلاستيك. درجة الحرارة الثابتة بشكل عام هي 200 درجة مئوية ، ولكن يمكن إجراء التعديل المناسب لأعلى / لأسفل وفقًا لطول زمن الأكسدة. وفقًا لاختلاف وقت استحثاث الأكسدة (OIT) لدفعات مختلفة من العينات ، يمكن مقارنة اختلاف المواد المضادة للأكسدة للمواد وتأثير مضادات الأكسدة المختلفة للإضافات المضادة للأكسدة ، ويمكن استخدامها بشكل غير مباشر لتحديد اختلاف خصائص المواد المضادة للشيخوخة. معايير القياس ذات الصلة: DIN EN 728 ، ISO / TR 10837 ، ASTM D 3895.
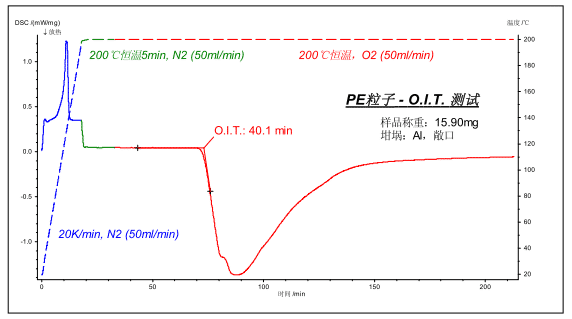
توضح الصورة أعلاه اختبار OIT لجسيمات البلاستيك البولي إيثيلين وفقًا للطريقة القياسية الوطنية. تم وزن العينة إلى حوالي 15 مجم ، ووضعت في بوتقة Al المفتوحة ، ودُفنت حتى 200 درجة مئوية تحت حماية 50 مل / دقيقة N 2 ، وتحولت إلى O 2 بعد 5 دقائق. كانت فترة استحثاث الأكسدة المقاسة (الفارق الزمني من التحول الأولي إلى O2 إلى نقطة بدء الاستقراء لذروة الأكسدة الطاردة للحرارة) 40.1 دقيقة.
8. اختبار المعالجة
يمكن لـ DSC قياس عملية المعالجة لراتنجات بالحرارة (مثل راتنجات الايبوكسي ، الراتنجات الفينولية ، إلخ) ، وكذلك الطلاء والمواد اللاصقة وما شابه.
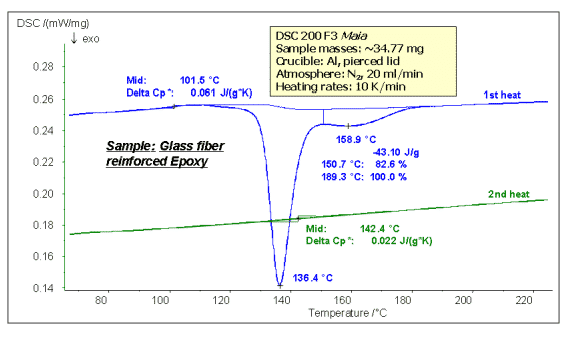
يوضح الشكل التالي اختبار المعالجة بارتفاع درجة الحرارة لراتنج الإيبوكسي المقوى بالألياف الزجاجية (GFEP). درجة حرارة التزجج غير المعالجة غير المعالجة (101.5 درجة مئوية) وتتصلب أثناء عملية التسخين. يظهر ذروة كبيرة للحرارة على منحنى DSC (136.4 ، 158.9 درجة مئوية ذروة مزدوجة في الشكل ، علاج المحتوى الحراري 43.10) J / g) ؛ بعد التبريد لارتفاع درجة الحرارة الثانية ، حيث تماسك الراتينج ، ترتفع درجة حرارة التزجج إلى 142.4 درجة مئوية ، ولا تظهر ذروة المعالجة الحرارية.
ملاحظة: بالنسبة لراتنجات الايبوكسي ، تكون درجة حرارة التزجج قريبة من الخطية لدرجة المعالجة. كلما زادت درجة المعالجة ، كلما كان التشابك الداخلي للمادة أكثر اكتمالًا ، انخفض حركة المقطع ، وارتفعت درجة حرارة التزجج.
9. اختبار تغير المرحلة
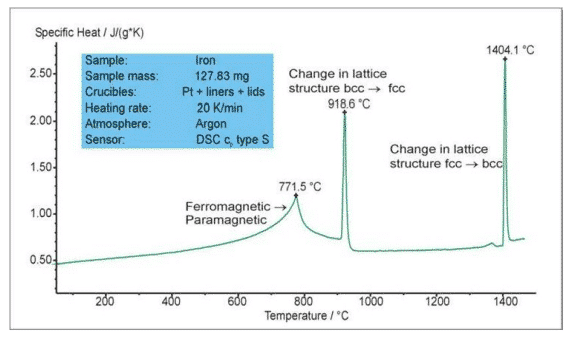
يوضح الشكل أعلاه اختبار تغيير الطور للحديد أثناء عملية التسخين. الذروة الماصة للحرارة عند 771.5 درجة مئوية هي انتقال نقطة كوري ويتم تحويل المادة من مغناطيس حديدي إلى مغناطيسي مغناطيسي. الذروة الماصة للحرارة عند 918.6 درجة مئوية و 1404.1 درجة مئوية هي الانتقال بين هيكلين شبكيين (مركز جسم مخفي - مركز وجه لجنة الاتصالات الفدرالية). يتميز Netzsch SC404 / STA449 بهيكل محكم عالي التفريغ ونظام تفريغ آلي بالكامل مع نظام فريد لامتصاص الأكسجين OTS لضمان قياس العينات في جو خامل نقي لتجنب الأكسدة في درجات حرارة مرتفعة.
10. تعدد الأشكال
يشير تعدد الأشكال إلى الظاهرة القائلة بأن المادة يمكن أن توجد في هيكلين بلوريين مختلفين أو أكثر. أشكال الكريستال المختلفة لها خصائص فيزيائية وكيميائية مختلفة ويمكن تحويلها إلى بعضها البعض تحت ظروف معينة.

يوضح الشكل أعلاه قياس DSC للدواء Sulfathiazole. الذروة الماصة للحرارة عند 173.7 درجة مئوية في الشكل هي ذوبان الصيغة III ، والتي يتم تحويلها بعد ذلك إلى الشكل الأول. الذروة الماصية للحرارة عند 196.2 درجة مئوية هي ذوبان الشكل الثاني ، والذروة الماصة للحرارة عند 201.4 درجة مئوية هي ذوبان النموذج الأول.
11. اختبار الحرارة المحدد
مبدأ الاختبار
وفقًا لتعريف الفيزياء الحرارية ، فإن السعة الحرارية النوعية c (السعة الحرارية النوعية الحرارية الثابتة Cp المشاركة في التحليل الحراري العام) هي الطاقة المطلوبة لزيادة درجة حرارة الوحدة لكل وحدة كتلة للعينة عند درجة حرارة معينة. وهي: Cp = Q / (m * △ T) ، الوحدة J / g * K
قم بتغيير هذه المعادلة قليلاً:
س = Cp * m * △ T.
ثم قم بتمييز الوقت ، خذ الطاقة الماصة للحرارة للعينة أثناء عملية التسخين q = dQ / dt ، معدل التسخين HR = dT / dt ، أي: q = Cp * m * HR
باستخدام نوع تدفق الحرارة DSC ، يتم قياس الطاقة الماصة للحرارة q لعينة الحرارة المحددة غير المعروفة sam وعينة الحرارة القياسية المحددة المعروفة std عند درجة حرارة معينة على التوالي بنفس معدل التسخين في معدل تسخين ديناميكي ، ويتم الحصول عليها:
Qsam = KT * (DSCsam - DSCbsl) = Cpsam * msam * HR
Qstd = KT * (DSCstd - DSCbsl) = Cpstd * mstd * HR
KT هو معامل الحساسية لمستشعر تدفق الحرارة ، والذي من خلاله يمكن تحويل إشارة DSC الأصلية (وحدة الأشعة فوق البنفسجية) عند درجة حرارة معينة إلى إشارة تدفق الحرارة (وحدة mW). DSCbsl هو خط أساس يتم قياسه باستخدام زوج من الفراغات ويتم خصمه عند قياس التدفق الحراري للعينة والمعيار.
اقسم المعادلتين أعلاه ، ويتم تقسيم KT و HR على بعضهما للحصول على:
(DSCsam - DSCbsl) / (DSCstd - DSCbsl) =
(Cpsam * msam) / (Cpstd * mstd)
تغيير طفيف ، أي السعة الحرارية المحددة للضغط المستمر للعينة عند درجة حرارة معينة:
Cpsam = Cpstd × [(DSCsam - DSCbsl) / msam] / [(DSCstd - DSCbsl) / mstd] = Cpstd × DSCsam ، rel ، sub / DSCstd ، rel ، sub
حيث يمثل DSCxxx ، rel ، sub إشارة DSC بعد طرح خط الأساس أو المرجع من خط الأساس في الإحداثيات النسبية ، μV / mg.
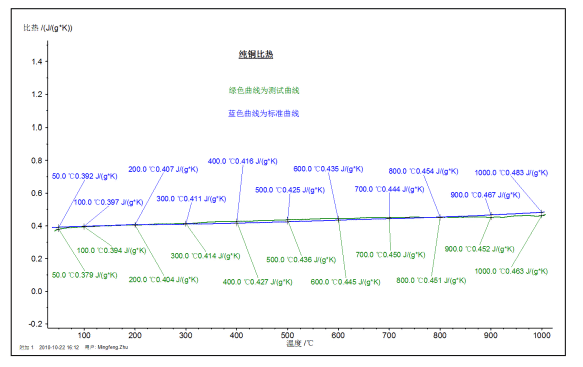
يوضح الشكل أعلاه القيمة الحرارية المحددة (المنحنى الأخضر) لعينة من النحاس النقي المقاسة عند درجة حرارة عالية DSC في نطاق RT ~ 1000 درجة مئوية ، والمقارنة مع قيمة الأدب (المنحنى الأزرق).







عمل رائع جداً.