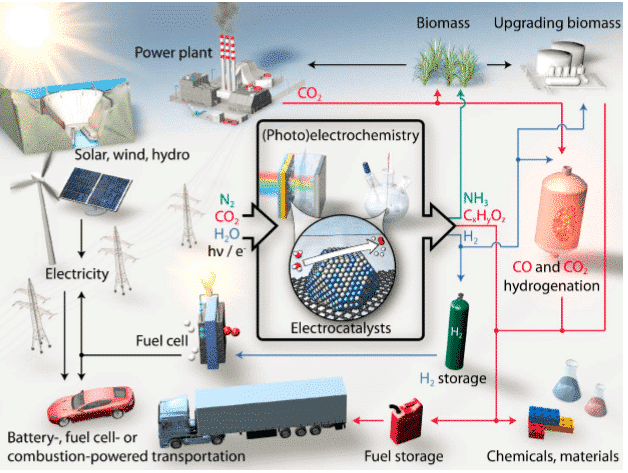
La technologie de réaction électrocatalytique est l'une des méthodes clés qui conduisent ces voies de conversion d'énergie et de purification de l'environnement.
Ces dernières années, avec le développement de la société et les progrès de l'humanité, les problèmes énergétiques et environnementaux de plus en plus graves sont devenus un problème mondial qui doit être résolu de toute urgence. Les gens sont déterminés à utiliser efficacement les nouvelles sources d'énergie et les méthodes de purification à long terme de l'environnement. Les méthodes de recherche efficaces actuelles pour promouvoir la conversion d'énergie et la purification de l'environnement impliquent de nombreuses directions, telles que le développement des piles à combustible, la production d'hydrogène, les ressources en CO2, la conversion catalytique organique des gaz d'échappement. Les méthodes d'essai électrochimique en tant que guide théorique fournissent un moyen rationnel d'interprétation pour le développement des performances de l'électrocatalyseur. Cet article résume les méthodes d'essai électrochimique couramment utilisées dans plusieurs réactions électrochimiques.
Figure 1 Processus électrocatalytique de conversion d'énergie durable
1. voltampérométrie cyclique
La voltampérométrie cyclique (CV) est la méthode de recherche la plus couramment utilisée pour évaluer les systèmes électrochimiques inconnus. Il est principalement obtenu en contrôlant le potentiel d'électrode à différentes vitesses et en balayant une ou plusieurs fois avec une forme d'onde triangulaire dans le temps. Courbe potentiel-courant (iE). Différentes réactions de réduction et d'oxydation peuvent se produire alternativement sur les électrodes dans différentes plages de potentiel. La réversibilité de la réaction des électrodes peut être jugée en fonction de la forme de la courbe; les pics d'adsorption et de désorption des réactifs peuvent être utilisés pour évaluer l'électrocatalyseur en fonction de la plage de potentiel spécifique. La zone catalytiquement active peut également être utilisée pour obtenir des informations utiles sur les réactions d'électrodes complexes.
Figure 1.1 Balayage de la courbe de réponse potentielle actuelle
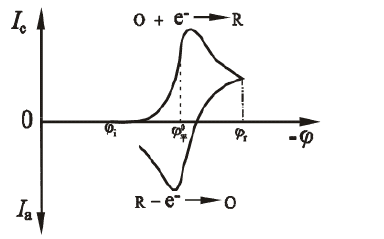
Comme le montre la figure 1.1, le potentiel de la première moitié est balayé vers la cathode, et la substance électroactive est réduite sur l'électrode pour générer une onde de réduction. Lorsque le potentiel de cette dernière moitié est balayé vers l'anode, le produit de réduction est à nouveau oxydé sur l'électrode pour générer une onde d'oxydation. Deux paramètres utiles de la courbe de voltampérométrie iE sont le rapport de courant de crête ipa / ipc et la différence de potentiel de crête Epa-Epc. Pour l'onde de Nernst du produit stable, le rapport de courant de crête ipa / ipc = 1, indépendamment de la vitesse de balayage, du coefficient de diffusion et du potentiel de commutation. Lorsque le balayage cathodique est arrêté, le courant est dégradé à 0, puis inversé scand. La courbe iE obtenue est exactement la même que la courbe cathodique, mais est dessinée dans le sens opposé de la coordonnée I et de la coordonnée E. Le rapport ipa / ipc s'écarte de 1, indiquant que le processus d'électrode n'est pas un processus de réaction entièrement réversible impliquant une cinétique homogène ou d'autres complications. La hauteur et la surface du pic de réaction peuvent être utilisées pour estimer les paramètres du système tels que la concentration d'espèces électroactives ou la constante de vitesse de la réaction homogène couplée. Cependant, la courbe CV n'est pas une méthode quantitative idéale, et son utilisation puissante est davantage dans sa capacité de jugement semi-quantitatif qualitatif.
2. voltampérométrie par impulsion
La voltampérométrie pulsée est une méthode de mesure électrochimique basée sur le comportement des électrodes polarographiques. Il est utilisé pour étudier le processus redox dans divers milieux, l'adsorption de matériaux de surface sur des matériaux catalyseurs et le mécanisme de transfert d'électrons à la surface d'électrodes chimiquement modifiées. La détection est particulièrement efficace. La voltampérométrie à impulsions comprend la voltampérométrie à étapes, la voltampérométrie à impulsions conventionnelle, la voltampérométrie à impulsions différentielle et la voltampérométrie à onde carrée selon la façon dont la tension est balayée. Parmi eux, la voltampérométrie pas à pas est similaire à la méthode de balayage potentiel, et la réponse de la plupart des systèmes au voltampère pas à résolution plus élevée (ΔE <5 mV) est très similaire aux résultats de l'expérience de balayage linéaire de la même vitesse de balayage.
3. Spectroscopie d'impédance électrochimique
La spectroscopie d'impédance électrochimique consiste à appliquer un signal électrique perturbé au système électrochimique. Contrairement à la méthode de balayage linéaire, le système électrochimique est loin de l'état d'équilibre, puis la réponse du système est observée, et les propriétés électrochimiques du système sont analysées par le signal électrique de réponse. La spectroscopie d'impédance électrochimique est souvent utilisée pour analyser, évaluer la réaction ORR dans les piles à combustible PEM, caractériser la perte de diffusion à la surface du matériau catalyseur, estimer la résistance ohmique et les caractéristiques de l'impédance de transfert de charge et de la capacité à double couche pour évaluer et optimiser l'ensemble électrode à membrane.
Le spectre d'impédance est généralement dessiné sous la forme d'un diagramme de Bode et d'un diagramme de Nyquist. Dans le diagramme de Bode, l'amplitude et la phase de l'impédance sont tracées en fonction de la fréquence; dans le diagramme de Nyquist, la partie imaginaire de l'impédance est tracée à chaque point de fréquence par rapport à la partie réelle. L'arc haute fréquence reflète la combinaison de la capacité à double couche de la couche de catalyseur, de l'impédance de transfert de charge efficace et de la résistance ohmique, qui reflète l'impédance produite par transfert de masse. Pour un système donné, les deux régions sont parfois mal définies.
Figure 3.1 Spectre d'impédance du système électrochimique
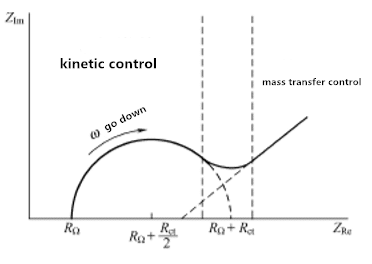
La figure 3.1 montre les caractéristiques extrêmes du contrôle cinétique et du contrôle de transfert de masse. Cependant, pour un système donné, les deux régions ne sont probablement pas bien définies. Le facteur déterminant est la relation entre la résistance de transfert de charge et l'impédance de transmission. Si le système chimique est lent en cinétique, il affichera un grand Rct, qui semble avoir une région de fréquence très limitée. Lorsque le système est dynamique, le transfert de matière joue toujours un rôle de premier plan et les zones semi-circulaires sont difficiles à définir.
4. chronoampérométrie
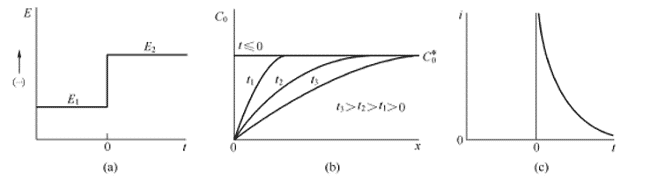
La méthode de la chronoampérométrie est une méthode de contrôle transitoire qui peut être utilisée pour évaluer l'adsorption et la diffusion de la surface du catalyseur. La courbe de chronoampérométrie est obtenue en appliquant une étape de potentiel au système électrochimique pour mesurer la variation du signal de réponse courant dans le temps. Lorsqu'une étape potentielle est donnée, la forme d'onde de base est représentée sur la figure 4.1 (a), et la surface de l'électrode solide est analysée avec un matériau électroactif. Après l'application de l'étape potentielle, les espèces électroactives près de la surface de l'électrode sont d'abord réduites en un radical anion stable, qui nécessite un courant important car le processus se produit immédiatement à l'instant de l'étape. Le courant circulant ensuite est utilisé pour maintenir les conditions dans lesquelles le matériau tensioactif d'électrode est complètement réduit. La réduction initiale provoque un gradient de concentration (c'est-à-dire la concentration) entre la surface de l'électrode et la solution en vrac, et le matériau actif commence ainsi à diffuser en continu vers la surface et à diffuser vers l'électrode. La matière active sur la surface est complètement réduite immédiatement. Le flux de diffusion, c'est-à-dire le courant, est proportionnel au gradient de concentration de la surface de l'électrode. Cependant, il est à noter qu'au fur et à mesure que la réaction se déroule, le matériau actif dans la solution en vrac diffuse en continu vers la surface de l'électrode, provoquant une extension progressive de la région du gradient de concentration vers la solution en vrac, et le gradient de concentration en surface de l'électrode solide progressivement devient plus petit (épuisé) et le courant change progressivement. petit. La distribution des concentrations et le courant en fonction du temps sont présentés dans les figures 4.1 (b) et 4.1 (c).
Figure 4.1 (a) Forme d'onde expérimentale par étapes, le réactif O ne réagit pas au potentiel E1, est réduit à E2 à la vitesse limite de diffusion; (b) la distribution des concentrations à différents moments; (c) Courant en fonction du temps
5. technologie d'électrode à disque rotatif
La technologie d'électrode à disque rotatif (RDE) est très utile pour étudier la réaction homogène couplée de la surface du catalyseur, de sorte que la réaction électrochimique à la surface du catalyseur est effectuée dans un état relativement stable. Le RDE peut contrôler les substances à diffusion plus lente, comme le gaz qui se diffuse facilement dans la solution, réduisant ainsi l'influence de la couche de diffusion sur la distribution de densité de courant. Ainsi, une densité de courant stable est obtenue, qui est dans un état stationnaire approximatif, ce qui est bénéfique pour le processus d'analyse électrochimique; Le RDE peut contrôler la vitesse à laquelle l'électrolyte atteint la surface de l'électrode en ajustant la vitesse de rotation et mesurer les paramètres du processus de réaction électrocatalytique à différentes vitesses de rotation. une analyse.
Alors que les humains s'intéressent de plus en plus au développement d'électrocatalyseurs avancés pour la conversion d'énergie propre, en plus de mettre l'accent sur l'utilisation de certaines méthodes de base pour la caractérisation des réactions électrocatalytiques, un examen plus approfondi des étapes élémentaires de chaque réaction est nécessaire pour déterminer les implications. les intermédiaires, la surface de l'intermédiaire et l'énergie de chaque étape de réaction élémentaire. L'étude des méthodes électrochimiques nécessite encore de nombreux détails sur l'interface électrode-électrolyte qui n'étaient pas connus jusqu'à présent, tels que la cinétique et les barrières de réaction impliquées dans les étapes élémentaires clés du transfert proton / électron; près des solvants, des cations et des interfaces de réaction. La description de l'état atomique au niveau moléculaire de l'anion; et les méthodes d'acquisition de signaux en temps réel plus rapides et plus efficaces tout au long du processus de réaction électrochimique sont toujours à l'avant-garde des réactions électrocatalytiques. En résumé, une étude approfondie des méthodes de caractérisation électrochimique fournit une stratégie directrice pour le développement de nouveaux systèmes de catalyseurs à haut rendement.