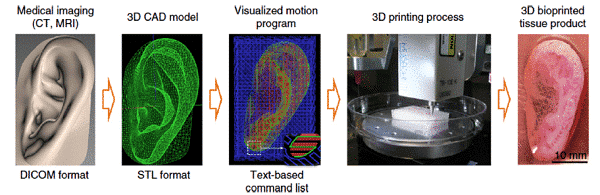
積層造形、ラピッド プロトタイピング技術、フリーフォーミング技術などとしても知られる 3 次元プリンティング (3DP) は、コンピューター支援のレイヤリングおよび重ね合わせ成形技術を使用した個別スタッキングの原理に基づいています。マテリアルはレイヤーごとに追加され、3D ソリッドが形成されます。 1986 年にチャールズ W. ハルによって 3D プリンティング技術の概念が初めて提案されて以来、3D プリンティングはあらゆる分野に浸透し、イノベーションを導き、その高精度、個別化された製造、および複雑な形状の構築における独自の利点により、世界的な製造業をもたらしました。 。業界の変化。生物学的 3D プリンティングは、生物医学分野における 3D プリンティング技術の相互応用であり、重要な研究的意義と応用の見通しを持っています。 3D プリンティング技術を使用して、標準モデルだけでなく、患者向けにオーダーメイドの外科用ステントも作成できます。患者の骨欠損をコンピューター断層撮影 (CT) や核磁気共鳴 (MRI) などの医用画像技術でスキャンして、目的のステント モデルを取得し、3 次元プリンターで印刷します。これは、従来の成形技術では達成することが困難です。近年、3D プリンティング技術は、頭蓋顔面移植、歯冠修復、補綴装置、医療機器、手術モデル、臓器プリンティング、薬物送達モデル、骨組織工学ステントなどを含む医療分野で広く使用されています [1]。 3D プリンティング技術は、そのカスタマイズ性、構造および細孔の制御性、および複数の材料を複合できる能力により、研究者から幅広い注目を集めています。この傾向は、画期的な治療法や装置を備えた多くの発明にも影響を与えました。
次に、骨組織工学の分野で現在3D印刷に利用できる生体材料について、それぞれの長所と短所、印刷基準などを詳しく説明します。同時に、プリンタごとに異なる生体材料を印刷できるため、3Dプリンタの種類と成形原理の概要も示します。このレビューにより、より多くの研究チームが新しい生体材料を発明し、最終的には3Dプリント技術を骨組織工学の分野でさらに発展させることが期待されます。
1. 3D印刷技術分類の概要
生体材料を印刷できるかどうかは、使用する3Dプリンターに大きく関係します。プリンタごとに素材要件は異なります。生物医学の分野で使用される主なプリンターは、光硬化ステレオ印刷技術、溶融蒸着印刷技術、選択的レーザー焼結技術、直接スラリー押出技術の4つのタイプに分類されます。
融合沈着と直接スラリー押出技術は、骨組織工学足場を準備するために一般的に使用される2つの方法です。一部の直接印刷されたペーストは、水または低沸点溶媒(ジクロロメタン(DCM)、ジメチルスルホキシド(DMSO))と混合されたポリマーソリューションです。一部は、押出後すぐに蒸発するポリマーソリューションです。または一部のヒドロゲルは、押出後も元の構造を保持します。三次元印刷によって形成され、チキソトロピー挙動、温度検知、または押し出し後の架橋によって形状を維持できます。溶融蒸着および直接印刷の場合。XY平面での解像度は25ミクロンまで可能で、層厚さは200〜500ミクロンです。[2]一般に、サポートされていない、または鋭利な長いモデルを印刷する場合、これらの2つの方法には問題があります。フィラメントには十分な強度がないため、すぐにサポートできません。サポートされていないパーツです。この問題を解決するために、印刷が完了した後、印刷プロセス中に充填材が追加される場合があります。充填材は溶剤または高温でか焼。
粒子溶解3D印刷技術は、選択的レーザー焼結蒸着技術や粒子接着技術を含む産業用プロトタイピングで広く使用されており、ポリマー、セラミック、金属、およびそれらの複合材料を印刷するだけでなく、独自のまたは複雑な構造を提供します。選択的レーザー焼結では、特定の方向のレーザーを使用して、ポリマーまたは金属粒子を融点より高くし、それによって粒子を一緒に溶融します。コンピューターモデルに従ってレーザービームが重ねられ、粒子が上から溶かされ、この手順が繰り返されて最終結果が得られます[3]。選択的レーザーテクノロジーは、作成に時間がかかり、コストが高く、大量の材料を使用する必要がありますが、単一の工作機械で複数の材料を形成できるため、多くの製造分野でヒットしています。粒子結合技術は無指向性レーザー焼結技術とも呼ばれ、その主な原理は選択的レーザー焼結技術と同様です。しかしながら、粒子のレーザー溶融とは異なり、粒子結合技術は、液体結合剤溶液を使用して粒子を結合し、次いで高温か焼によって三次元固体を得る。選択的レーザー焼結技術と粒子接着技術は、整形外科や口腔外科などの硬組織工学で使用されています。
ステレオリソグラフィーは、光重合性液体ポリマーを通して紫外光またはレーザー光を形成して、単一の硬質ポリマーフィルムを形成するプロセスです。重合後、新しい樹脂が印刷面上を流れて上で重合できるように、基板は溶液に降ろされます。すべての印刷技術の中で、ステレオリソグラフィは最高の解像度を持ち、従来のステレオリソグラフィの解像度は25ミクロンに達しますが、マイクロスケールのステレオリソグラフィと高精度のステレオリソグラフィはシングルミクロンの解像度を持ちます[4]]。ただし、ステレオリソグラフィーにより、紫外線の下でのみ架橋でき、拡張されたポストフォーミング特性、適切な機械的特性の欠如、樹脂が最後に簡単にブロックされ、最も重要なのはステレオリソグラフィーに使用できる関連する生物学的相が欠けていることです。 。容量性で生分解性の素材のため、医療分野での開発の余地がありません。しかしながら、近年、いくつかの天然または合成の架橋可能な生体材料の発見は、組織工学の分野におけるステレオリソグラフィーの適用に大きな機会を提供している[5]。
図1耳の印刷方法[6]
2.三次元印刷生物医学材料分類
過去10年の間に3Dプリンティング技術は急速に発展し、多くの新しい分野への応用を可能にし、医療機器やティッシュエンジニアリングの注目を集めてきました。 3Dプリンティングは特定の医療製品を患者に合わせて短時間で低コストで調整できるため、3Dプリンティングテクノロジーは将来の個人医療の時代に大きな発展の見通しを持っています。現在、三次元印刷により骨組織工学の足場や他の医療製品を準備するための多くの生物学的材料があります。このセッションでは、さまざまな印刷技術に必要な材料特性の概要を説明し、適用された生体材料とその長所と短所を強調します。
2.1セラミックベースのスラリー
バイオメディカルアクティブセラミックは、天然の骨のミネラル相、構造、機械的特性をシミュレートすることにより、バイオニック骨修復材料に最適です。液体セラミック材料は数が少なく、その融点は溶融蒸着印刷が耐えられる範囲をはるかに超えているため、現在3Dプリンターを使用してセラミック材料を直接印刷することは困難です。さらに、セラミック材料は、感光特性がないため、光硬化性の3次元印刷技術には適していません。また、選択的レーザー焼結印刷システムを使用して高密度の多孔性構造を印刷することも困難です。直接押出3D印刷技術は現在、セラミック材料を印刷するための最も有望な方法です。セラミックパウダーは、印刷を容易にするために、適切な粒子サイズ(通常は10〜150ミクロン)と適切な接着剤が必要です。成形[7]。
ヒドロキシアパタイトパウダーは、3次元印刷で広く使用されています。これは、ミネラル相に含まれる大量のリン酸カルシウムに関連しています。ポリアクリル酸溶液をHAパウダー上に1層ずつスパッターした後、焼結して硬化プロセスを完了し、ヒドロキシアパタイトカップリングを得ました。焼結により、その圧縮強度(0.5-12Mpa)はヒトの海綿骨の最小要件を満たすことができます。マウスモデルに移植し、8週間後、ステントの端で骨の新生が始まり、内部に類骨と血管が成長した。しかしながら、人工骨足場の優れた性能にもかかわらず、それはまだ臨床使用基準からほど遠いです[8]。バイオガラスは、内部分子がランダムに配置されたケイ酸塩の集合体です。材料の構成要素は、生体の構成要素と交換または反応して、生物自体と適合性のある物質を形成します。研究者は、細胞および動物実験を通じて生物活性ガラスに関する一連の研究を実施し、バイオガラスは優れた自己分解性を有し、そのイオン生成物は骨芽細胞の増殖と分化を増強し、骨形成遺伝子の発現を活性化できることを発見しました。 Lu et al [9]は、腫瘍関連の骨欠損疾患を効果的に治療するために、最初に磁性ナノ粒子修飾メソポーラスバイオガラスを調製し、それをキトサンと混合して、多孔質複合足場を調製しました。複合足場は、良好な骨再生と光熱療法機能を備えており、腫瘍関連の骨欠損の治療に大きな応用価値があります。
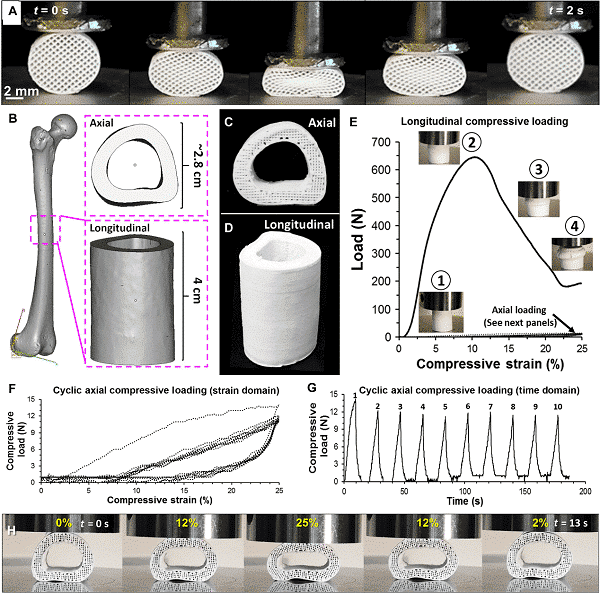
図2超弾性人工骨[10]
2.1医用高分子材料
医療用ポリマー印刷材料は、優れた処理特性を備え、さまざまな印刷モードに適用でき、生体適合性と分解性が優れているため、3D印刷の生体材料の主力となっています。異なる印刷技術では、異なる材料の印刷パラメータを設定する必要があります。たとえば、溶融蒸着印刷では、熱可塑性ポリマー材料が使用されます。これは、原料をフィラメントの形状に引っ張るだけで印刷できますが、その直径は通常約1.75 mmであり、固溶体変換の特性が速いため、絞られています。外に出る前に素早く溶け、押し出し後にすばやく冷却できます。光硬化三次元印刷技術では、スラリーが液体状態であり、感光特性を持っている必要があります。
現在、最も広く使用されている三次元印刷ポリマー材料は、ポリ乳酸(PLA)やポリカプロラクトン(PCL)などの分解性脂肪族ポリエステル材料です。ポリカプロラクトンは、ティッシュエンジニアリングと3Dプリンティングの登場までかつては捨てられていた半結晶性ポリマーであり、PCLは再び歴史的な段階にあります。ポリカプロラクトンは、優れたレオロジー特性と加熱時の粘弾性特性を備えており、溶融蒸着に基づくプリンターにとって最も重要な材料の1つです。ポリカプロラクトンは体内で最大6か月間安定しており、その後徐々に分解されます。また、副産物は人体に無害で無害です。ポリ乳酸は、生体適合性と生分解性に優れた線状熱可塑性脂肪族ポリエステルです。しかしながら、ポリ乳酸の分解はエステル結合の加水分解によって達成されるため、乳酸の放出は周囲の体液環境におけるpH値の低下を引き起こす。これらの酸性副産物は、組織の炎症や細胞死を起こしやすいです。この問題を改善するために、研究者らはポリ乳酸とバイオセラミックを組み合わせて、生体反応性を改善し、酸性環境の形成を妨げる複合足場を準備しました。 Ion et al [11]は、3D印刷技術を使用して、皮質および海綿骨の特性に一致する新しいアパタイト-ウォラストナイト/ポリ乳酸(AW / PLA)複合構造を製造しました。インビトロ細胞実験の結果は、AW / PLA複合足場がラット骨髄由来間葉系幹細胞の増殖および骨形成分化を効果的に促進できることを示した。ラットの頭蓋骨欠損モデルでは、複合足場は良好なオッセオインテグレーションと新しい骨形成を促進する能力を示しました。
PLAおよびPCLに加えて、ポリプロピレン(PPF)は、光硬化において最も研究されている生分解性および光架橋性ポリマー材料の1つです。通常、印刷されたペーストはフマル酸ジエチルDEF溶剤と混合され、光開始剤も追加されます。溶液の粘度とPPFとDEFの比率は、印刷プロセスとステントの機械的特性に大きな影響を与えます。ポリエーテルエーテルケトン(PEEK)は、350°Cの融点があるため、選択的レーザー焼結印刷技術によってのみ形成できます。ただし、融点が高いため、PEEKに耐熱性があり、高温蒸気滅菌時に安定します。しかし、PPEKは生体材料として、組織工学に適したオッセオインテグレーションがなく、天然の骨とうまく組み合わせることができないため、拒絶反応が発生しやすく、価格が高くなります[12]。
2.3ヒドロゲルスラリー
ヒドロゲルは、水溶性高分子を化学架橋または物理架橋してなる高分子であり、三次元架橋網目構造を有しており、水自体も多量に含まれている。ヒドロゲルは、調整可能な強度、分解性、機能的修飾などの特性を備えており、細胞外マトリックスの微小環境を模倣する軟質材料として使用できるため、ヒドロゲルは医療分野で幅広いアプリケーションの見通しを持っています。それは、二次元または三次元の組織工学足場および薬物の制御放出を準備するために使用することができます。一般的に使用される3次元印刷されたヒドロゲルペーストは、主に3つのカテゴリに分類されます。1つはアルギン酸、寒天、ゼラチン、セルロース、コラーゲン、絹フィブロイン、ヒアルロン酸などの天然ポリマーから調製されます。1つのタイプは、合成ポリマーなどから調製されます。ポリアクリルアミド、ポリウレタン、ポリエチレングリコールなど;もう1つは、合成ポリマーと天然ポリマーで構成された複合ヒドロゲルベースのスラリーです。
水溶性合成高分子の中でも、医療用ポリビニルアルコール(PVA)は、組織工学の分野で広く使用されています。 PVAは優れた生体適合性を持ち、非毒性で分解しやすく、95°Cで水に溶解でき、ゲルを形成し、粘度が高くなります。 Zhang et al [13]は、相互接続された細孔を備えたMBG / PVA複合足場を準備しました。 PVAの添加により、材料の靭性が大幅に向上しました。ラット頭蓋骨欠損モデルを使用した動物実験では、MBG / PVA足場が優れた骨誘導活性を有し、骨欠損での新しい骨形成と血管新生を促進することも示されました。
現在、細胞が3Dプリントされたバイオスキャフォールドと共培養される多くの実験があります。結果はまた、細胞がさまざまな3次元の足場で生存でき、通常の2次元の培養よりも優れていることも示しています。しかし、これはセルとマテリアルの2次元効果にすぎず、セルを印刷システムに直接配置することはありません。新しいアイデアとして細胞と印刷用ペーストを直接混合することも、研究者の間で広く注目されています。天然のヒドロゲルは、細胞適合性が良好です。その組成は細胞外基質と類似しており、表面のタンパク質や細胞に付着する能力が弱く、細胞の代謝過程にほとんど影響を与えません。細胞を包み込み、栄養素を輸送し、代謝産物を分泌します。アンドレア等。 [14] I型コラーゲンとヒアルロン酸のバイオインク配合をさまざまな比率でテストし、生物活性をサポートしながらバイオプリンティングを可能にし、ネイティブの細胞-マトリックス相互作用をサポートする最適な配合を決定しました。 。彼らはこの処方を、ヒト初代肝細胞と肝星細胞を含む3D肝組織の構築に適用し、一般的な肝毒性物質であるアセトアミノフェンの効果をテストしました。結果は、メチルメタクリレートコラーゲンとチオールヒアルロン酸の組み合わせが、間葉系細胞の成長を調節し、薬物を治療するシンプルで印刷可能なバイオインクを生成することを示しています。適切な反応をします。
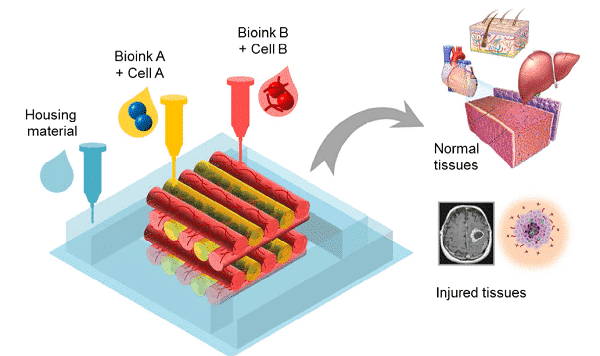
図3細胞のバイオプリンティング
3.結論と展望
3次元プリンティング技術は大きな応用の可能性を秘めていますが、バイオメディカル分野の主役としてはまだ解決すべき課題が多くあります。問題の 1 つは、3D プリンター自体の機能の制限にあります。印刷速度や印刷精度は大幅に向上しましたが、依然として最高のレベルに達していない場合が多くあります。もう 1 つの大きな問題は、代替生体材料の限界です。印刷できる多くの材料にはそれぞれ独自の利点がありますが、移植に使用される材料は生理学的条件の要件を満たし、人体への良好な反応性を備えている必要があります。一般に、理想的な整形外科用材料には、(1) 印刷適性、(2) 生体適合性、(3) 優れた機械的特性、(4) 良好な分解性、および (5) 副生成物の特性が必要です。非毒性かつ分解性、(6) 良好な組織生体模倣特性。プリンタの種類が異なれば材料要件も異なり、これらの特性を完全に満たすことが難しい場合があります。例えば、骨組織工学では、骨芽細胞の増殖や負荷に対応するために高強度の足場材料が必要となる一方で、足場が劣化しにくいという問題も生じる。強度が低く柔らかい材質の中には印刷が容易で劣化しやすいものもありますが、負荷のかかる部分には適用できません。一般に、3 次元プリントされたペーストは、その独自の硬度と自然な骨の近接性により、骨および軟骨の修復の分野で使用されます。基本的に、生体材料の選択は、所望の材料を達成するためにそれらの性能のバランスを取ることです。
ポリマーバイオスラリーは、特にPLAやPCLなどの安価なエラストマーを対象に、幅広く研究されています。これらの材料は、優れた生体適合性と機械的特性を備えており、基板材料として広く使用されています。これらに加えて、将来の研究では、ポリマー材料の分解性、脆性、および細胞適合性に注意を払う必要があります。 HAやβ-TCPなどのセラミック材料は、伝統的に硬組織工学の足場に理想的な材料と考えられており、セラミックとポリマーの複合材料の研究でますます使用されています。セラミック材料の追加を改善できます。ステントの強度と複合材料の生物学的特性。ハイドロゲルバイオスラリーとプリンティングシステムの開発により、多機能の細胞搭載モデルシステムのプリンティングに近づき、臓器プリンティングが実現することを期待しています。このプロセスは、超分子ヒドロゲルスラリーの研究から始まりました。最後に、3D印刷技術を医療分野に適用する場合、大量生産の方法、品質の管理方法、管理の障害を克服する方法はすべて解決する必要のある問題です。正面道路は長くなっていますが、3Dプリントは最終的にティッシュエンジニアリングと医学の分野で輝きます。
参照
[1]マーフィーSV、アタラA.組織および臓器の3Dバイオプリンティング[J]。 Nature Biotechnology、2014、32(8):773-785。
[2]グベンディレンM、モルデJ、ソアレスRMDなど。 3Dプリンティング用の生体材料の設計[J]。 ACSバイオマテリアルサイエンス&エンジニアリング、2016年。
[3]バーミューレンM、クラエッセンスT、ヴァンデアスミッセン、ヴァンホルスベーク、デバッカー、ヴァンランスベーク、ヴェルドンク。融合沈着モデリングによる患者固有の光学的にアクセス可能な気道モデルの製造。 Rapid Prototyping Journal 2013、19(5)、312-318。
[4]ベルトランドP、ベイルF、クームC、グーリオットP、スムロフI.選択的レーザー焼結によるセラミックコンポーネントの製造。アプリケーションサーフィン。サイエンス。 2007、254(4)、989-992。
[5]ダービーB.組織と足場の印刷とプロトタイピング[J]。サイエンス、2012、338(6109):921-6。
[6]カン、H.-W .;リー、SJ; Ko、IK;ケングラ、C;ユ、JJ; Atala、A.構造的完全性を備えた人間規模の組織構造を生成する3Dバイオプリンティングシステム。 Nat。バイオテクノロジー。 2016、34(3)、312-319。
[7] Xiaoyu Du、Shengyang Fu、Yufang Zhu。骨組織工学のためのセラミックベースの足場の3Dプリンティング:概要。ジャーナルオブマテリアルズケミストリーB、2018、6:4397-4412。
[8] Fierz FC、Beckmann F、Huser Mなど。異方性3Dプリントされたヒドロキシアパタイト足場の形態。バイオマテリアル、2008、29(28)、3799-3806。
[9] Jiawei Lu、Fan Yang、Qinfei Ke、Xuetao Xie、Yaping Guo。骨再生および腫瘍に対する光熱療法のための磁性ナノ粒子修飾多孔質足場。ナノ医療、2018、14(3):811-822
[10] AE ジャクス、AL ラッツ、SW ジョーダン、A. カナン、SM ミッチェル、C. ユン、KD コウベ、SC ヨー、HE ホワイトリー、CP リヒター、RD ガリアーノ、WK スー、SR ストック、EL スー、RN シャー、超弾性「骨」: 汎用性が高く、成長因子を含まず、骨再生性があり、拡張性があり、外科手術に適した生体材料、Sci Transl Med、2016、8:358。
[11] Ion Tcacencu、Natacha Rodrigues、Naif Alharbi、Matthew Benningなど。3D印刷技術を使用して作成された多孔質アパタイト-ウォラストナイトとポリ乳酸の複合構造のオッセオインテグレーション。 Mater Sci Eng C Mater Biol Appl、2018、90:1-7。
[12] Hoath S. D、Vadillo D. C、Harlen O. G、McIlroy C、Morrison N. F、Hsiao W. K、Tuladhar T. R、Jung S、Martin G. D、Hutchings IM弱いインクジェット印刷弾性ポリマー溶液。 J.非ニュートン流体機械。 2014、205、1-10。
[13]張、JH;趙、SC;朱、YF;黄、YJ;朱M;タオ、CL; Zhang、CQ骨再生用のストロンチウム含有メソポーラス生物活性ガラス足場の3次元印刷。 Acta Biomater。 2014、10(5)、2269−2281。
[14]アンドレア・マゾッキ、マヘシュ・デヴァラセッティ、リチャード・ハントワーク、シェイ・ソッカー、アレクサンダー・スカルダル。 3Dバイオプリント肝微小環境のためのコラーゲンタイプI-ヒアルロン酸ハイブリッドバイオインクの最適化。バイオファブリケーション、2018、11(1):015003。