في العقود الأخيرة ، جذبت بطاريات الليثيوم أيون الانتباه في مجال مواد الطاقة. في الوقت نفسه ، مع تطور النظرية الأساسية ومجال الكمبيوتر ، تم تطبيق العديد من طرق المحاكاة الحسابية في البحث عن بطاريات الليثيوم أيون. بسبب الأخطاء في العملية التجريبية ، فإن المقاييس المجهرية ، مثل آلية نمو أغشية SEI ، وديناميات انتشار الأيونات في مواد القطب ، وتطور الهياكل أثناء شحن وتفريغ مواد القطب ، والعلاقة بين الإمكانات والبنية ، و لا يمكن حل توزيع طبقات الشحنات الفضائية. استنتاجات بديهية ، لا يمكن للطرق التجريبية أن تعطي تفسيرًا نظريًا واضحًا. في المقابل ، تتمتع طرق المحاكاة الحسابية بمزايا نسبية في فهم تطور الكيمياء الداخلية والكيمياء الكهربية لبطاريات الليثيوم أيون. تتحقق الحسابات النظرية من النتائج التجريبية لمواد بطارية ليثيوم أيون ، كما تعزز وتوجه تطوير مواد البطاريات. نقدم أدناه العديد من طرق الحساب التناظرية الشائعة الاستخدام وتطبيقاتها في بطاريات الليثيوم أيون.
تطبيق نظرية الكثافة الوظيفية
تم استخدام نظرية الكثافة الوظيفية على نطاق واسع في أبحاث بطارية أيون الليثيوم. يستخدم بشكل شائع لحساب الاستقرار الهيكلي ، وإمكانية إدخال الليثيوم ، والهيكل الإلكتروني ، ونطاق الطاقة ، وهيكل الاسترخاء ، وطاقة توليد الخلل ، ومسار الهجرة ، وطاقة التنشيط والليثيوم. خصائص مثل حركية نقل الأيونات وإزالة التداخل في انتقالات طور الليثيوم.
قيمة الجهد للبطارية هي معلمة مرتبطة بتغيير في الطاقة الحرة لتفاعل البطارية. المواد المختلفة لها إمكانية إدراج الليثيوم الكامنة. تتمتع مادة القطب بشكل مثالي بإمكانية أعلى للإلكترود الموجب ، وإمكانية أقل للقطب السالب ، وفرق جهد بين الأقطاب الكهربائية المختلفة. يمكن حساب طاقة بطارية ليثيوم أيون وفقًا لاستجابة البطارية: (يتم التعبير عن قوة 1 مول من الإلكترون بواسطة F ، والطاقة الإلكترونية للإلكترون هي
1.602 × 10−19 C) F = NA · e− = 96487.56 درجة مئوية / مول
لنفترض أن n هو عدد الشحنات المنقولة أثناء تفاعل البطارية ، ثم تكون البطارية من خلال البطارية nF ، والحد الأقصى للعمل الكهربائي الذي تقوم به البطارية هو:
−Wr'=nFVAVE
في ظل ظروف متساوية الحرارة ، فإن طاقة جيبس الحرة للنظام تساوي العمل الذي يقوم به النظام للعالم الخارجي:
ΔG=−Wr'
ΔG = nFVAVE , ولأن Li + به وحدة شحن ، VAVE = ΔG / F
ΔG هي طاقة Gibbs الخالية من تفاعل البطارية ، على افتراض أن التغيير في الحجم والنتروبيا الناجم عن تفاعل تضمين الخلية لا يكاد يذكر ، إذن
G≈ΔE
لذلك : VAVE = ΔE / F.
بالنسبة لنظام البطارية الذي يكون فيه القطب الموجب هو LiA والقطب السالب هو B ، فمن المفترض أن يتم إزالة الليثيوم x من LiA ودمجها في B بعد الشحن (عملية الشحن الإيجابية) ، وصيغة التفاعل هي:
LiA + B → Li1 − xA + LixB
متوسط الجهد لهذه العملية هو الفرق بين طاقة كل حالة نهائية مقابلة من الليثيوم (Li1 − xA ، LixB) والحالة الأولية (LiA ، B) ، ثم الجهد:
V = [E (Li1 − xA) + E (LixB) −E (LiA) −E (B)] / xe
عندما يكون القطب السالب هو الليثيوم المعدني ، فيمكن تبسيطه على النحو التالي:
V = [E (Li1 − xA) + E (Lix) −E (LiA)] / xe
من خلال حساب الطاقة الإجمالية لكل مادة قبل وبعد التفاعل ، يمكن حساب جهد القطب وفقًا للصيغة أعلاه. ومع ذلك ، بالنسبة لجميع مواد الكاثود تقريبًا ، يكون الجهد المحسوب بواسطة نظرية الكثافة الوظيفية منخفضًا. من خلال تطبيق تصحيح + U على GGA القياسي ، أي طريقة GGA + U ، أو باستخدام HSE06 الوظيفي الهجين ، يمكن الحصول على جهد أقرب إلى القيمة التجريبية. في حساب مواد كاثود الأكسيد التي تحتوي على أيونات فلزية انتقالية ثلاثية الأبعاد ، تم التعرف على تأثير الارتباط القوي كتأثير يجب أخذه في الاعتبار.
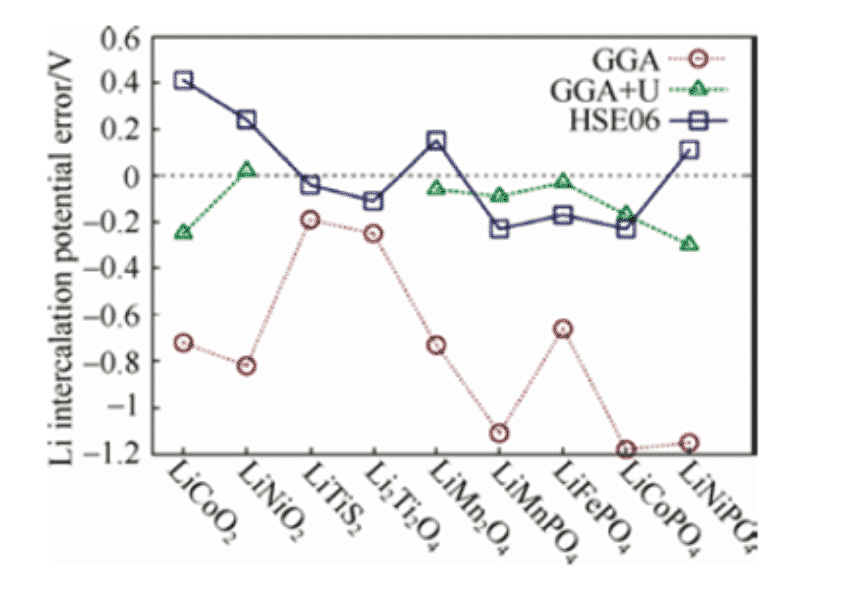
الشكل 1: معيار GGA و GGA + U ، HSE06 احسب أيونات الليثيوم المختلفة
طريقة الديناميكا الجزيئية
يمكن لحساب المبادئ الأولى على أساس الكثافة الوظيفية الحصول على خصائص المادة في حالة الأرض ذات درجة الحرارة الصفرية. يمكن دراسة نقل الذرات والأيونات في المادة عن طريق محاكاة الديناميات الجزيئية عند درجة حرارة محدودة. يستخدم حساب الديناميات الجزيئية كطريقة محاكاة على المستوى الذري باستخدام دالة محتملة تجريبية. بالمقارنة مع طريقة المبادئ الأولى ، يمكنها إجراء محاكاة على نطاق واسع ، والتي يمكنها عرض عملية الانتشار الديناميكي لأيون الليثيوم بشكل أفضل وتحليلها.
يمكن للديناميات الجزيئية محاكاة تطور جسيمات النظام بمرور الوقت ، وإلقاء نظرة على مسار هجرة الأيونات ، وحساب معامل انتشار الجسيمات واستقرار المواد ، لكن قانون حركة الجسيمات هو ميكانيكا نيوتن ، ووجود جسيمات منخفضة الجودة مثل الهيدروجين والهيليوم تأثير حساب التأثير الكمي ليس مثاليًا. فيما يتعلق ببطاريات الليثيوم أيون ، يمكن للديناميات الجزيئية الحصول على معامل الانتشار ومسار انتقال الأيونات في المواد ، مما يوفر لنا إمكانية فهم آلية انتشار الأيونات في المواد.
قام Yang بحساب عملية الانتشار الذاتي لـ LiFePO4 ووجد أن هجرة Li + في المادة لا تحدث بشكل مستمر ، ولكنها تحدث من خلال الانتقال بين مواقع الشبكة المجاورة. في عام 2014 ، استخدم Zhang Jungan وآخرون من جامعة شنغهاي الديناميكيات الجزيئية لمحاكاة سلوك انتشار أيونات الليثيوم بين طبقات الجرافيت أثناء الشحن. تمت دراسة خصائص انتشار أيون الليثيوم لمواد أنود الجرافيت عند 300 كلفن. توفر النتائج التجريبية بيانات أساسية لدراسة نموذج المقياس المستمر لتشوه قطب بطارية أيون الليثيوم.
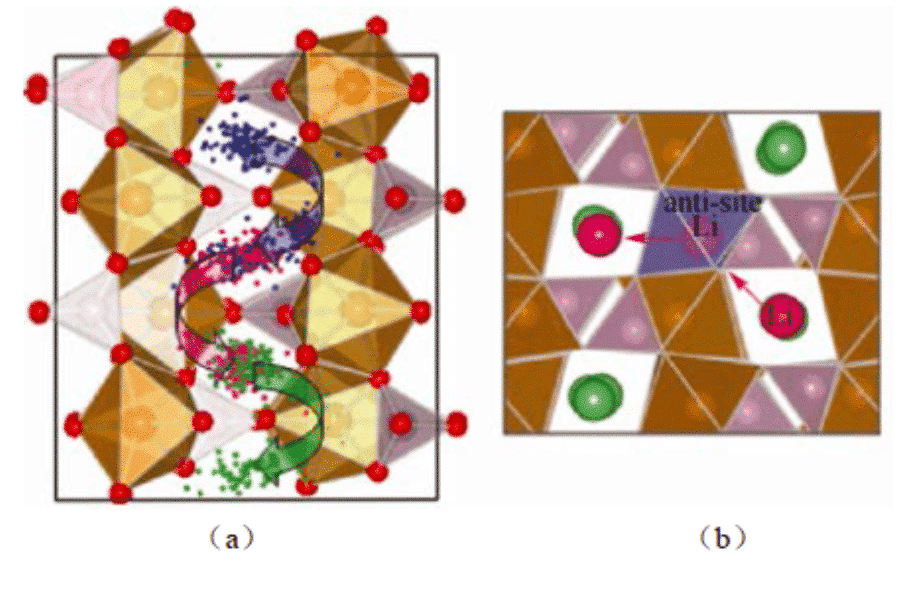
الشكل 2: تظهر محاكاة الديناميات الجزيئية (أ) مسار أيونات Li في LiFePO4 ؛ (ب) هجرة أيونات Li بين القنوات من خلال عيوب احتلال Li / Fe المتبادلة
نموذج حقل المرحلة
تعتمد طريقة حقل الطور على نظرية Ginzburg-Landau. تُستخدم المعادلة التفاضلية لتمثيل الانتشار ، وترتيب الجهد والمحرك الديناميكي الحراري لآلية فيزيائية محددة. يتم حل المعادلات أعلاه عن طريق برمجة الكمبيوتر. ادرس الحالة الآنية للنظام في الزمان والمكان. يعتمد نموذج حقل الطور على المبادئ الأساسية للديناميكا الحرارية والديناميات وهو أداة قوية للتنبؤ بتطور البنى المجهرية أثناء تحولات طور الحالة الصلبة.
يمكن لنموذج حقل الطور محاكاة نمو البلورات ، وتحول الطور الصلب ، وتطور الشقوق ، وانتقال طور الفيلم ، وهجرة الأيونات في الواجهة ، وما إلى ذلك ، ولكن نتائج المحاكاة تفتقر إلى المقارنة الكمية مع مراقبة الوقت. عادة ما يتم تعيين سمك الواجهة أكبر من الوضع الفعلي. مما أدى إلى نقص التفاصيل. نشر Marnix Wagemaker (المؤلف المراسل) من جامعة Delft للتكنولوجيا في هولندا مقالاً في مجلة Adv.Funct.Mater. في عام 2018 لاقتراح نموذج حقل طور ديناميكي حراري لإدخال أيونات الليثيوم في الإسبنيل Li4Ti5O12 ، مع دمج بيانات DFT. توفر القدرة على وصف السلوك الديناميكي الحراري الكامل للجسيمات المنفصلة عن الطور اتجاهًا محددًا لتصميم أفضل أداء للقطب الكهربي Li4Ti5O12.
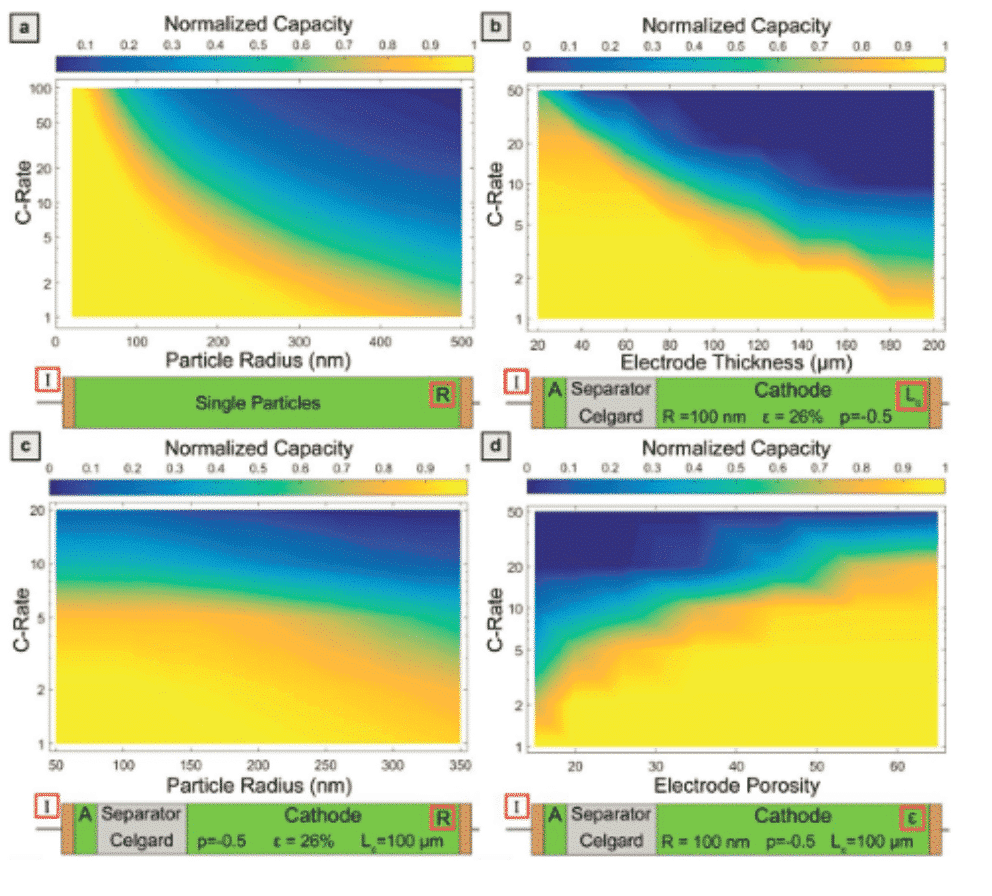
الشكل 3: محاكاة جسيم واحد LTO ، العلاقة بين سعة البطارية وسعة التفريغ الاسمية وسماكة القطب تحت محاكاة القطب المسامي
طريقة العناصر المحدودة
طريقة العناصر المحدودة هي تقنية عددية لحل مشكلة القيمة الحدية للمعادلات التفاضلية الجزئية. يكون تدفق محاكاة طريقة العناصر المحدودة على النحو التالي: 1. تحديد منطقة مشكلة الحل 2. تحديد متغير الحالة وطريقة التحكم المتغيرة للمنطقة ، أي معادلة تطور الفضاء الزمني المتغير. 3. قم باشتقاق الوحدة المفردة ، وقم بتجميع الوحدة. تم حل الحل الشامل ، وأخيرًا تم حل المعادلات الآنية والحصول على النتائج.
من أجل فهم أفضل لسلوك التسخين الزائد لبطاريات الليثيوم أيون ذات السعة الكبيرة والطاقة العالية للسيارات الكهربائية، استخدم Cao Binggang من جامعة Xi'an Jiaotong طريقة العناصر المحدودة لمحاكاة درجة الحرارة الداخلية للبطارية أثناء النظر في المقاومة الداخلية. الحمل الحراري والتبديد الخارجي. التوزيع المكاني ونتائج محاكاة توزيع درجة الحرارة لخلية الاختبار في فرن ساخن بدرجة حرارة 155 درجة مئوية وتكوين البطارية VLP50/62/100S-Fe (3.2 فولت/55 أمبير·ساعة) LiFePO4/جرافيت.
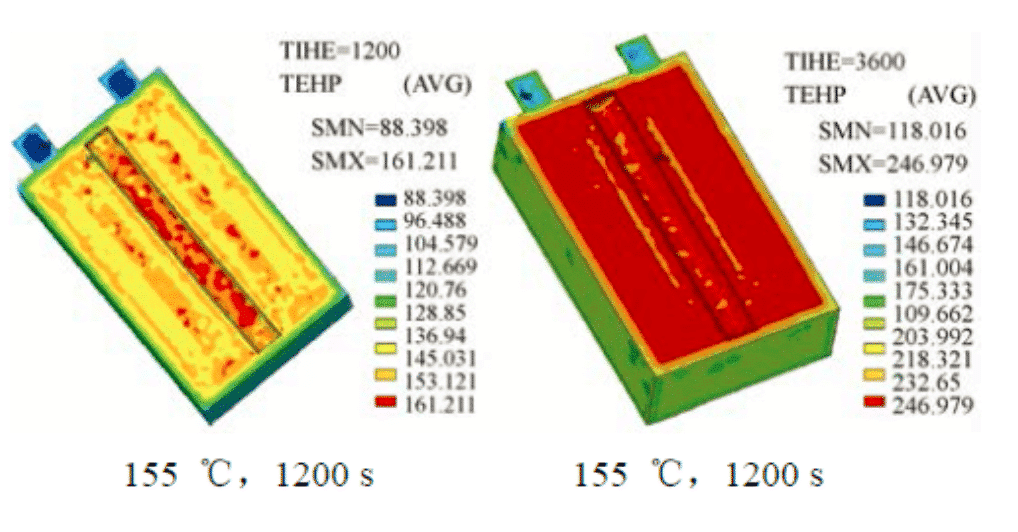
الشكل 4: توزيع محاكاة العناصر المحدودة في الخلية عند 155 درجة مئوية و 1200 ثانية و 3600 ثانية
تركز عمليات محاكاة المواد العيانية مثل نماذج حقل الطور وطرق العناصر المحدودة على القضايا الهندسية وتساعد على فهم الظواهر العيانية مثل الإجهاد ونقل الحرارة والتدفق والاقتران متعدد المجالات في بطاريات الليثيوم أيون. يعد حساب المبادئ الأولى المستند إلى نظرية الكثافة الوظيفية أكثر ملاءمة للخصائص الفيزيائية الدقيقة مثل الطاقة والبنية الإلكترونية لنظام المواد.
مع تطور النظرية والتطبيق المكثف لمحاكاة الكمبيوتر ، سيقود علم المواد الحسابية ويتحقق من علم المواد التجريبية. سيعزز الحساب من النطاق العياني إلى النظرية المجهرية بشكل كبير تطوير مجال المواد لبطاريات الليثيوم أيون. من حيث العديد من المشاكل في العلوم التجريبية ، بمساعدة المحاكاة الحسابية ، سيكون أيضًا تفسيرًا نظريًا واضحًا. سيؤدي فهم طرق المحاكاة الحسابية لبطاريات الليثيوم أيون إلى تسريع تطوير وتطبيق مواد بطاريات الليثيوم أيون.
المرجعي:
[1] هوانغ جي ، ولينج شيغانغ ، ووانغ زويلونغ ، وآخرون. مشكلة العلوم الأساسية لبطارية ليثيوم أيون (XIV) —- طريقة الحساب [J]. علوم وتكنولوجيا تخزين الطاقة ، 2015 ، 4 (2): 215-230.
[2] جي شيانغ ، سونغ ييتشينغ ، تشانغ جونجان. محاكاة الديناميكيات الجزيئية لخصائص انتشار Li_xC_6 في بطاريات ليثيوم أيون [J]. مجلة جامعة شنغهاي (العلوم الطبيعية) ، 2014 (1): 68-74.
[3] شي سيقي (السيسي كي). دراسة المبادئ الأولى لمواد الكاثود لبطاريات الليثيوم أيون [D]. بكين: معهد الفيزياء الأكاديمية الصينية للعلوم ، 2004. [4] آليات انتشار أيون Yang JJ Tse J S. Li في LiFePO4 : دراسة ديناميكية جزيئية abinitio [J]. J. فيز. علم. أ , 2011-115 (45 13045-13049.
[5] فاسيلياديس أ ، كليرك إن جي دي ، سميث آر بي ، وآخرون. نحو الأداء الأمثل والفهم العميق لأقطاب الإسبنيل Li4Ti5O12 من خلال نمذجة حقل الطور [J]. مواد وظيفية متقدمة ، 2018.
[6] هيرزمان سي ، جونتر جي ، إيكر ب ، وآخرون. نمذجة العناصر الحرارية المحدودة ثلاثية الأبعاد لبطارية ليثيوم أيون في تطبيق الإساءة الحرارية [J]. مجلة مصادر الطاقة ، 2010 ، 195 (8): 2393-2398.